Descubre la tabla periódica: organización y estructura
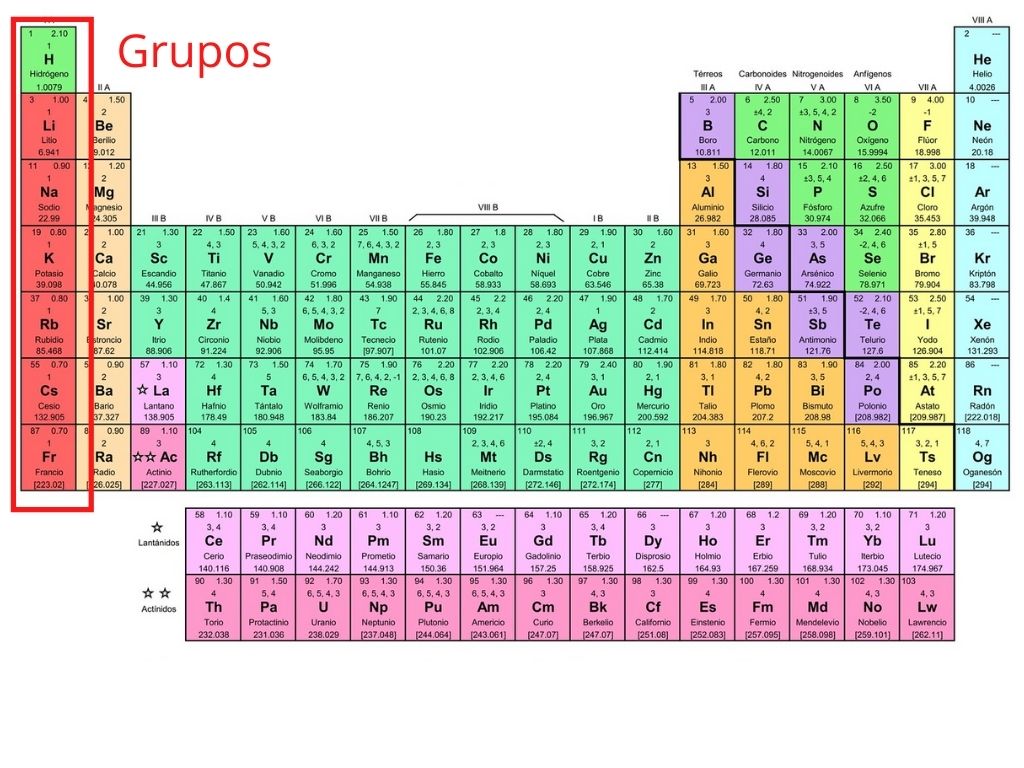
La tabla periódica es una herramienta fundamental en el estudio de la química, ya que nos permite entender la organización y estructura de los elementos químicos. En esta tabla, los elementos se ordenan según su número atómico y se agrupan en filas y columnas según sus propiedades químicas y físicas. En este artículo, te explicaremos todo lo que necesitas saber sobre la tabla periódica.
¿Qué es la tabla periódica?
La tabla periódica es una representación gráfica de todos los elementos químicos conocidos. Fue creada por el químico ruso Dmitri Mendeléyev en 1869 y desde entonces ha sido utilizada por científicos de todo el mundo para clasificar y estudiar los elementos.
La tabla periódica se divide en filas horizontales llamadas periodos y columnas verticales llamadas grupos. Los elementos se colocan en la tabla periódica según su número atómico, que es el número de protones que tiene un átomo en su núcleo.
Organización de la tabla periódica
La tabla periódica se organiza en periodos y grupos. Los periodos son las filas horizontales de la tabla periódica y están numerados del 1 al 7. Los elementos en un mismo periodo tienen el mismo número de orbitales electrónicos.
Los grupos son las columnas verticales de la tabla periódica y están numerados del 1 al 18. Los elementos en un mismo grupo tienen propiedades químicas y físicas similares.
Periodos en la tabla periódica
Los periodos de la tabla periódica se dividen en siete filas horizontales. Cada fila representa un nivel energético de los electrones. Los elementos en un mismo periodo tienen el mismo número de orbitales electrónicos.
Primer período
El primer período de la tabla periódica contiene sólo dos elementos: hidrógeno y helio. El hidrógeno es el elemento más ligero y abundante en el universo, mientras que el helio es un gas noble que se utiliza en globos y dirigibles.
Segundo período
El segundo período de la tabla periódica contiene ocho elementos: litio, berilio, boro, carbono, nitrógeno, oxígeno, flúor y neón.
Tercer período
El tercer período de la tabla periódica contiene ocho elementos: sodio, magnesio, aluminio, silicio, fósforo, azufre, cloro y argón.
Cuarto período
El cuarto período de la tabla periódica contiene dieciocho elementos, comenzando con el potasio y terminando con el kriptón.
Quinto período
El quinto período de la tabla periódica contiene dieciocho elementos, comenzando con el rubidio y terminando con el xenón.
Sexto período
El sexto período de la tabla periódica contiene dieciocho elementos, comenzando con el cesio y terminando con el radón.
Séptimo período
El séptimo período de la tabla periódica contiene treinta y dos elementos, comenzando con el francio y terminando con el oganesón.
Grupos en la tabla periódica
Los grupos en la tabla periódica son las columnas verticales que se utilizan para clasificar los elementos según sus propiedades químicas y físicas. Hay 18 grupos en la tabla periódica y cada uno tiene un número y un nombre.
Grupo 1: Metales alcalinos
Los metales alcalinos son los elementos del grupo 1 de la tabla periódica. Son metales blandos, altamente reactivos y tienen un solo electrón en su capa externa. Los metales alcalinos incluyen el litio, el sodio, el potasio, el rubidio, el cesio y el francio.
Grupo 2: Metales alcalinotérreos
Los metales alcalinotérreos son los elementos del grupo 2 de la tabla periódica. Son metales que tienen dos electrones en su capa externa y son menos reactivos que los metales alcalinos. Los metales alcalinotérreos incluyen el berilio, el magnesio, el calcio, el estroncio, el bario y el radio.
Grupo 3-12: Metales de transición
Los metales de transición son los elementos del grupo 3-12 de la tabla periódica. Son metales que tienen una alta densidad, punto de fusión y punto de ebullición. Los metales de transición tienen una mayor variedad de estados de oxidación que los metales alcalinos y alcalinotérreos.
Grupo 13: Grupo del boro
El grupo del boro es el grupo 13 de la tabla periódica. Incluye el boro, el aluminio, el galio, el indio y el talio. Estos elementos tienen tres electrones en su capa externa.
Grupo 14: Grupo del carbono
El grupo del carbono es el grupo 14 de la tabla periódica. Incluye el carbono, el silicio, el germanio, el estaño y el plomo. Estos elementos tienen cuatro electrones en su capa externa.
Grupo 15: Grupo del nitrógeno
El grupo del nitrógeno es el grupo 15 de la tabla periódica. Incluye el nitrógeno, el fósforo, el arsénico, el antimonio y el bismuto. Estos elementos tienen cinco electrones en su capa externa.
Grupo 16: Grupo del oxígeno
El grupo del oxígeno es el grupo 16 de la tabla periódica. Incluye el oxígeno, el azufre, el selenio, el telurio y el polonio. Estos elementos tienen seis electrones en su capa externa.
Grupo 17: Halógenos
Los halógenos son los elementos del grupo 17 de la tabla periódica. Son elementos altamente reactivos y tienen siete electrones en su capa externa. Los halógenos incluyen el flúor, el cloro, el bromo, el yodo y el astato.
Grupo 18: Gases nobles
Los gases nobles son los elementos del grupo 18 de la tabla periódica. Son elementos muy estables y no reactivos debido a que tienen una capa electrónica completa. Los gases nobles incluyen el helio, el neón, el argón, el criptón, el xenón y el radón.
Conclusion
La tabla periódica es una herramienta fundamental en el estudio de la química. Nos permite entender la organización y estructura de los elementos químicos y clasificarlos según sus propiedades químicas y físicas. Conocer la tabla periódica es esencial para cualquier estudiante de química, y esperamos que este artículo te haya ayudado a entender su organización y estructura.
Deja una respuesta