Descubre las características físicas del enlace covalente
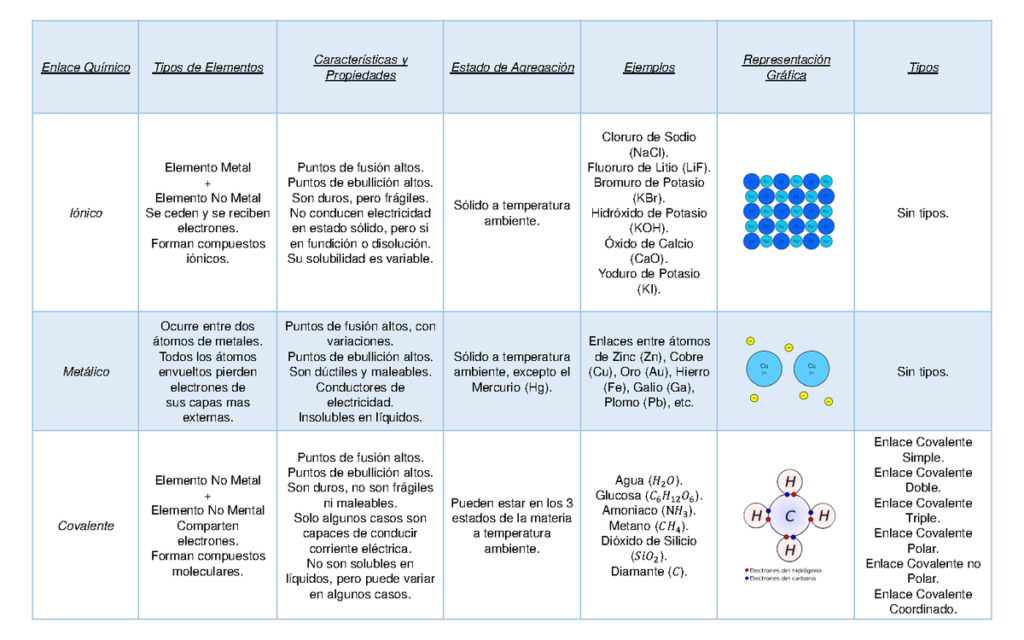
Los enlaces covalentes son uno de los tipos más comunes de enlaces químicos. Estos enlaces se forman cuando dos átomos comparten electrones para completar su capa de valencia. En esta ocasión, descubriremos las características físicas del enlace covalente.
- ¿Qué es un enlace covalente?
- Características físicas del enlace covalente
- Tipos de enlaces covalentes
- Conclusión
-
Preguntas frecuentes
- 1. ¿Qué es un enlace covalente?
- 2. ¿Cuál es la diferencia entre un enlace covalente no polar y un enlace covalente polar?
- 3. ¿Por qué los compuestos covalentes tienen puntos de fusión y ebullición bajos?
- 4. ¿Por qué los compuestos covalentes no conducen electricidad en estado sólido o líquido?
- 5. ¿Qué es un ejemplo de enlace covalente no polar?
¿Qué es un enlace covalente?
Un enlace covalente es una unión química en la que dos átomos comparten uno o más pares de electrones. Estos electrones son atraídos simultáneamente por los núcleos de los átomos, lo que crea una fuerza de enlace que mantiene los átomos unidos.
Características físicas del enlace covalente
Los enlaces covalentes tienen varias características físicas, incluyendo:
1. Punto de fusión y ebullición
Los compuestos covalentes tienen puntos de fusión y ebullición relativamente bajos en comparación con los compuestos iónicos. Esto se debe a que los enlaces covalentes son más débiles que los enlaces iónicos.
2. Solubilidad
Los compuestos covalentes son generalmente solubles en disolventes apolares, como el benceno, pero no son solubles en disolventes polares, como el agua. Esto se debe a que los compuestos covalentes son en general no polares.
3. Conductividad eléctrica
Los compuestos covalentes no conducen electricidad en estado sólido o líquido porque no tienen electrones libres que puedan moverse. Sin embargo, algunos compuestos covalentes pueden conducir electricidad cuando se disuelven en agua porque se disocian en iones y liberan electrones.
4. Dureza
Los compuestos covalentes son generalmente más blandos que los compuestos iónicos debido a su menor fuerza de enlace.
5. Estado de agregación
Los compuestos covalentes pueden existir en los tres estados de agregación: sólido, líquido y gaseoso.
Tipos de enlaces covalentes
Existen dos tipos de enlaces covalentes: enlace covalente no polar y enlace covalente polar.
Enlace covalente no polar
En un enlace covalente no polar, los átomos comparten electrones de manera equitativa. Esto significa que los átomos tienen la misma electronegatividad. Un ejemplo de enlace covalente no polar es el enlace entre dos átomos de hidrógeno.
Enlace covalente polar
En un enlace covalente polar, los átomos comparten electrones de manera desigual. Esto se debe a que los átomos tienen diferentes electronegatividades. Un ejemplo de enlace covalente polar es el enlace entre un átomo de hidrógeno y un átomo de cloro en el cloruro de hidrógeno.
Conclusión
Los enlaces covalentes son una forma importante de unión química. Tienen varias características físicas, incluyendo puntos de fusión y ebullición bajos, solubilidad en disolventes apolares y no conductividad eléctrica en estado sólido o líquido. Los enlaces covalentes también pueden ser no polares o polares dependiendo de la diferencia de electronegatividad entre los átomos.
Preguntas frecuentes
1. ¿Qué es un enlace covalente?
Un enlace covalente es una unión química en la que dos átomos comparten uno o más pares de electrones.
2. ¿Cuál es la diferencia entre un enlace covalente no polar y un enlace covalente polar?
En un enlace covalente no polar, los átomos comparten electrones de manera equitativa y tienen la misma electronegatividad. En un enlace covalente polar, los átomos comparten electrones de manera desigual debido a la diferencia de electronegatividad.
3. ¿Por qué los compuestos covalentes tienen puntos de fusión y ebullición bajos?
Los compuestos covalentes tienen puntos de fusión y ebullición bajos porque los enlaces covalentes son más débiles que los enlaces iónicos.
4. ¿Por qué los compuestos covalentes no conducen electricidad en estado sólido o líquido?
Los compuestos covalentes no conducen electricidad en estado sólido o líquido porque no tienen electrones libres que puedan moverse.
5. ¿Qué es un ejemplo de enlace covalente no polar?
Un ejemplo de enlace covalente no polar es el enlace entre dos átomos de hidrógeno.
Deja una respuesta