Descubre por qué la electronegatividad se incrementa en un periodo
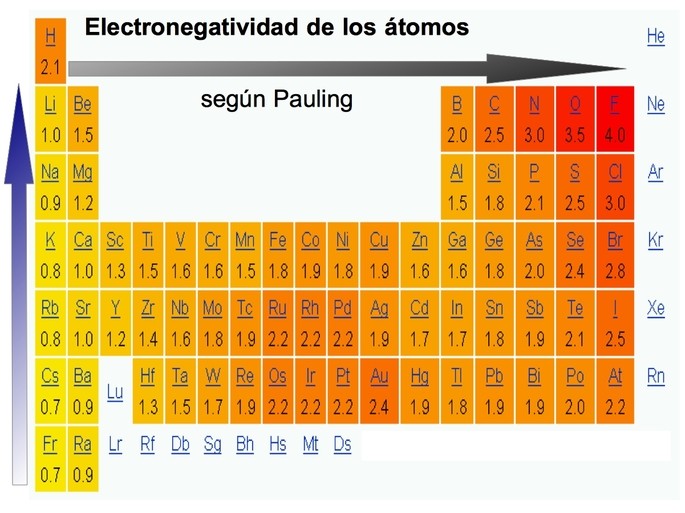
La electronegatividad es una propiedad química que mide la capacidad de un átomo para atraer los electrones hacia sí mismo cuando se encuentra en un enlace químico. Esta propiedad es muy importante, ya que determina la polaridad de los compuestos y su capacidad para formar enlaces químicos con otros átomos.
Una de las características más interesantes de la electronegatividad es que se incrementa en un periodo, es decir, cuando nos desplazamos de izquierda a derecha en la tabla periódica. ¿A qué se debe esto? En este artículo vamos a descubrir las razones detrás de este fenómeno.
- 1. ¿Qué es un periodo en la tabla periódica?
- 2. ¿Qué es la electronegatividad?
- 3. ¿Por qué la electronegatividad se incrementa en un periodo?
- 4. ¿Cómo afecta la electronegatividad a los enlaces químicos?
- 5. ¿Cómo influye la electronegatividad en las propiedades de los compuestos?
- 6. ¿Cómo se relaciona la electronegatividad con otras propiedades atómicas?
- 7. ¿Cómo se puede predecir la electronegatividad de un elemento?
- Conclusión
-
Preguntas frecuentes
- 1. ¿Qué es la carga nuclear efectiva?
- 2. ¿Por qué la electronegatividad es una propiedad importante en la formación de enlaces químicos?
- 3. ¿Qué es un enlace covalente polar?
- 4. ¿Cómo se relaciona la electronegatividad con el tamaño atómico?
- 5. ¿Cómo se puede predecir la electronegatividad de un elemento?
1. ¿Qué es un periodo en la tabla periódica?
Antes de entrar en detalles, es importante entender qué es un periodo en la tabla periódica. Un periodo es una fila horizontal en la tabla periódica que representa el número de orbitales que tiene el subnivel de mayor energía de los elementos que la componen. En otras palabras, los elementos de un mismo periodo tienen el mismo número de orbitales en su último nivel energético.
2. ¿Qué es la electronegatividad?
La electronegatividad es una propiedad química que mide la capacidad de un átomo para atraer los electrones hacia sí mismo cuando se encuentra en un enlace químico. Esta propiedad fue propuesta por Linus Pauling en 1932 y se mide en una escala que va del 0 al 4.
3. ¿Por qué la electronegatividad se incrementa en un periodo?
La electronegatividad se incrementa en un periodo porque a medida que nos desplazamos de izquierda a derecha en la tabla periódica, aumenta el número de protones en el núcleo atómico. Esto hace que la carga nuclear efectiva (es decir, la atracción que ejerce el núcleo sobre los electrones) aumente, lo que a su vez aumenta la electronegatividad.
4. ¿Cómo afecta la electronegatividad a los enlaces químicos?
La electronegatividad es una propiedad muy importante en la formación de enlaces químicos. Cuando dos átomos con electronegatividades diferentes se unen para formar un enlace, el átomo más electronegativo atrae los electrones hacia sí mismo, generando una polaridad en la molécula. Esto se debe a que el enlace se convierte en un enlace covalente polar, en el que los electrones se comparten de manera desigual.
5. ¿Cómo influye la electronegatividad en las propiedades de los compuestos?
La electronegatividad es una propiedad que influye en las propiedades físicas y químicas de los compuestos. Por ejemplo, los compuestos con una gran diferencia de electronegatividad entre sus átomos constituyentes tienden a tener puntos de fusión y ebullición más altos que los compuestos con una electronegatividad similar. Además, la polaridad de los compuestos influye en su solubilidad en diferentes solventes, lo que puede ser clave en procesos de extracción y purificación.
6. ¿Cómo se relaciona la electronegatividad con otras propiedades atómicas?
La electronegatividad está relacionada con otras propiedades atómicas, como el tamaño atómico y la energía de ionización. Por ejemplo, a medida que la electronegatividad aumenta, el tamaño atómico disminuye, ya que la carga nuclear efectiva se incrementa y atrae más fuertemente a los electrones. Además, la energía de ionización (es decir, la energía necesaria para arrancar un electrón de un átomo) aumenta a medida que la electronegatividad aumenta, ya que los electrones están más fuertemente ligados al núcleo.
7. ¿Cómo se puede predecir la electronegatividad de un elemento?
La electronegatividad de un elemento se puede predecir a partir de su posición en la tabla periódica. En general, los elementos más electronegativos se encuentran en la parte superior derecha de la tabla periódica, mientras que los menos electronegativos se encuentran en la parte inferior izquierda. Sin embargo, es importante tener en cuenta que la electronegatividad también está influenciada por otros factores, como la geometría molecular y la hibridación de orbitales.
Conclusión
La electronegatividad es una propiedad química muy importante que influye en la formación de enlaces químicos y en las propiedades de los compuestos. En un periodo de la tabla periódica, la electronegatividad se incrementa a medida que aumenta el número de protones en el núcleo atómico y, por lo tanto, la carga nuclear efectiva. Entender cómo funciona la electronegatividad nos permite predecir las propiedades de los compuestos y diseñar moléculas con propiedades específicas.
Preguntas frecuentes
1. ¿Qué es la carga nuclear efectiva?
La carga nuclear efectiva es la carga que siente un electrón en un átomo, teniendo en cuenta la atracción que ejercen los protones en el núcleo y la repulsión que ejercen los otros electrones en los niveles energéticos inferiores.
2. ¿Por qué la electronegatividad es una propiedad importante en la formación de enlaces químicos?
La electronegatividad es importante en la formación de enlaces químicos porque determina la polaridad de los enlaces y, por lo tanto, la polaridad de las moléculas resultantes. Esto influye en las propiedades físicas y químicas de los compuestos y en su capacidad para interactuar con otros compuestos.
3. ¿Qué es un enlace covalente polar?
Un enlace covalente polar es un enlace en el que los electrones se comparten de manera desigual entre los átomos que lo forman, debido a una diferencia de electronegatividad entre ellos.
4. ¿Cómo se relaciona la electronegatividad con el tamaño atómico?
A medida que la electronegatividad aumenta, el tamaño atómico disminuye, ya que la carga nuclear efectiva se incrementa y atrae más fuertemente a los electrones.
5. ¿Cómo se puede predecir la electronegatividad de un elemento?
La electronegatividad de un elemento se puede predecir a partir de su posición en la tabla periódica. En general, los elementos más electronegativos se encuentran en la parte superior derecha de la tabla periódica, mientras que los menos electronegativos se encuentran en la parte inferior izquierda.
Deja una respuesta