Descubre los factores que aceleran las reacciones químicas
Si alguna vez has cocinado algo en tu cocina, sabrás que hay ciertos factores que pueden acelerar el proceso de cocción, como la temperatura del horno, la cantidad de ingredientes y el tiempo de cocción. De manera similar, en la química existen varios factores que pueden acelerar el proceso de una reacción química.
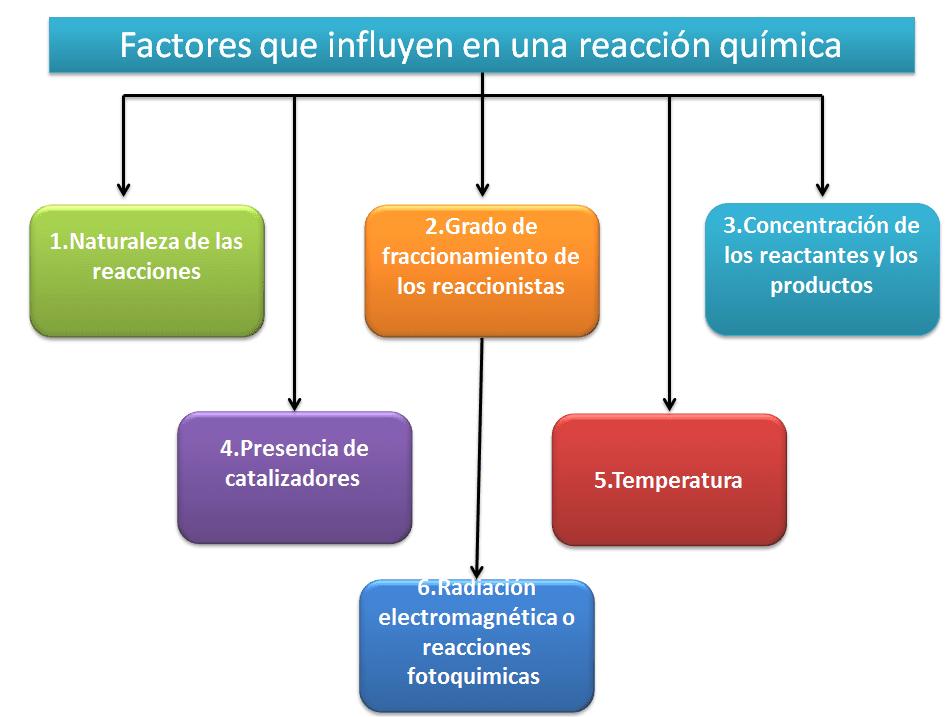
Las reacciones químicas ocurren cuando los átomos y moléculas interactúan para formar nuevas sustancias, y esta interacción puede ser acelerada o retardada por ciertos factores. A continuación, te presentamos los principales factores que aceleran las reacciones químicas.
- 1. Temperatura
- 2. Concentración de reactantes
- 3. Superficie de contacto
- 4. Catalizadores
- 5. Luz
- Conclusión
-
Preguntas frecuentes
- 1. ¿Qué factores pueden retardar una reacción química?
- 2. ¿Por qué los catalizadores son importantes en la industria?
- 3. ¿Cómo afecta la superficie de contacto la velocidad de una reacción química?
- 4. ¿Por qué la luz es importante para algunas reacciones químicas?
- 5. ¿Por qué es importante acelerar las reacciones químicas en la medicina?
1. Temperatura
La temperatura es uno de los factores más importantes que aceleran las reacciones químicas. Esto se debe a que las moléculas se mueven más rápido a temperaturas más altas, lo que aumenta la probabilidad de que colisionen y reaccionen entre sí. Por lo tanto, aumentar la temperatura de una reacción química puede acelerar su velocidad.
Por ejemplo, si colocas una taza de agua caliente en el congelador, el agua se enfriará más rápido que si la colocaras a temperatura ambiente. De manera similar, si aumentas la temperatura de una reacción química, la reacción se acelerará.
2. Concentración de reactantes
La concentración de los reactantes también puede afectar la velocidad de una reacción química. Si la concentración de los reactantes es alta, hay más moléculas presentes en un espacio determinado, lo que aumenta la probabilidad de que las moléculas colisionen y reaccionen entre sí. Esto acelera la velocidad de la reacción.
Por ejemplo, si agregas más sal al agua, la sal se disolverá más rápido que si agregas menos sal. De manera similar, si aumentas la concentración de los reactantes en una reacción química, la velocidad de la reacción aumentará.
3. Superficie de contacto
La superficie de contacto entre los reactantes también puede afectar la velocidad de una reacción química. Si los reactantes están en forma sólida, la reacción química solo puede ocurrir en la superficie de los sólidos. Por lo tanto, si aumentas la superficie de contacto entre los sólidos, la velocidad de la reacción aumentará.
Por ejemplo, si cortas una manzana en pedazos pequeños, se oxidará más rápido que si la dejas entera. De manera similar, si aumentas la superficie de contacto entre los reactantes en una reacción química, la velocidad de la reacción aumentará.
4. Catalizadores
Los catalizadores son sustancias que aceleran las reacciones químicas sin ser consumidos en la reacción. Los catalizadores funcionan al reducir la energía de activación necesaria para que la reacción ocurra. Esto hace que las moléculas reaccionen más fácilmente y acelera la velocidad de la reacción.
Por ejemplo, las enzimas son catalizadores biológicos que aceleran las reacciones químicas en nuestro cuerpo. De manera similar, los catalizadores pueden acelerar las reacciones químicas en un laboratorio.
5. Luz
La luz también puede acelerar algunas reacciones químicas. La luz puede proporcionar la energía necesaria para que la reacción ocurra. Por lo tanto, si la reacción química requiere energía de luz, la intensidad de la luz puede afectar la velocidad de la reacción.
Por ejemplo, la fotosíntesis es una reacción química que ocurre en las plantas y requiere luz para producir glucosa. La intensidad de la luz puede afectar la velocidad de la fotosíntesis.
Conclusión
Existen varios factores que pueden acelerar las reacciones químicas. La temperatura, la concentración de los reactantes, la superficie de contacto, los catalizadores y la luz pueden afectar la velocidad de una reacción química. Comprender estos factores es importante para controlar y acelerar las reacciones químicas en la industria, la medicina y la investigación.
Preguntas frecuentes
1. ¿Qué factores pueden retardar una reacción química?
La temperatura baja, la falta de catalizadores y la falta de reactantes pueden retardar una reacción química.
2. ¿Por qué los catalizadores son importantes en la industria?
Los catalizadores pueden acelerar las reacciones químicas en la industria, lo que a su vez puede reducir los costos y mejorar la eficiencia de los procesos químicos.
3. ¿Cómo afecta la superficie de contacto la velocidad de una reacción química?
Si los reactantes están en forma sólida, la reacción química solo puede ocurrir en la superficie de los sólidos. Por lo tanto, si aumentas la superficie de contacto entre los sólidos, la velocidad de la reacción aumentará.
4. ¿Por qué la luz es importante para algunas reacciones químicas?
La luz puede proporcionar la energía necesaria para que algunas reacciones químicas ocurran. Por lo tanto, la intensidad de la luz puede afectar la velocidad de la reacción.
5. ¿Por qué es importante acelerar las reacciones químicas en la medicina?
En la medicina, acelerar las reacciones químicas puede permitir la producción de medicamentos más rápido y más eficiente. También puede permitir la creación de nuevos métodos de diagnóstico y tratamiento.
Deja una respuesta