Descubre el significado de la 'S' en la tabla periódica
La tabla periódica es una herramienta fundamental en la química, ya que nos permite conocer las características y propiedades de los elementos químicos. Cada uno de ellos está representado por un símbolo, que a su vez tiene un significado específico. En este artículo vamos a centrarnos en la letra 'S' que aparece en la tabla periódica, y que tiene un importante significado en relación a los elementos químicos.
¿Qué es la letra 'S' en la tabla periódica?
La letra 'S' que aparece en la tabla periódica hace referencia a los orbitales s. Estos orbitales son los más cercanos al núcleo del átomo y tienen forma esférica. Los electrones que se encuentran en estos orbitales tienen la menor cantidad de energía de todos los electrones que se encuentran en los orbitales de un átomo.
¿Qué son los orbitales s?
Los orbitales s son los orbitales más cercanos al núcleo del átomo y tienen forma esférica. Estos orbitales son capaces de alojar hasta dos electrones, y se representan por un único símbolo. Los electrones que se encuentran en los orbitales s tienen la menor cantidad de energía de todos los electrones que se encuentran en los orbitales de un átomo.
¿Cuál es la importancia de los orbitales s?
Los orbitales s son importantes porque determinan la reactividad de los elementos químicos. Los electrones que se encuentran en los orbitales s son los más cercanos al núcleo y, por lo tanto, están más fuertemente atraídos por él. Esto significa que los elementos químicos que tienen electrones en los orbitales s son menos reactivos que los que tienen electrones en los orbitales p, d o f.
¿Qué elementos químicos tienen electrones en los orbitales s?
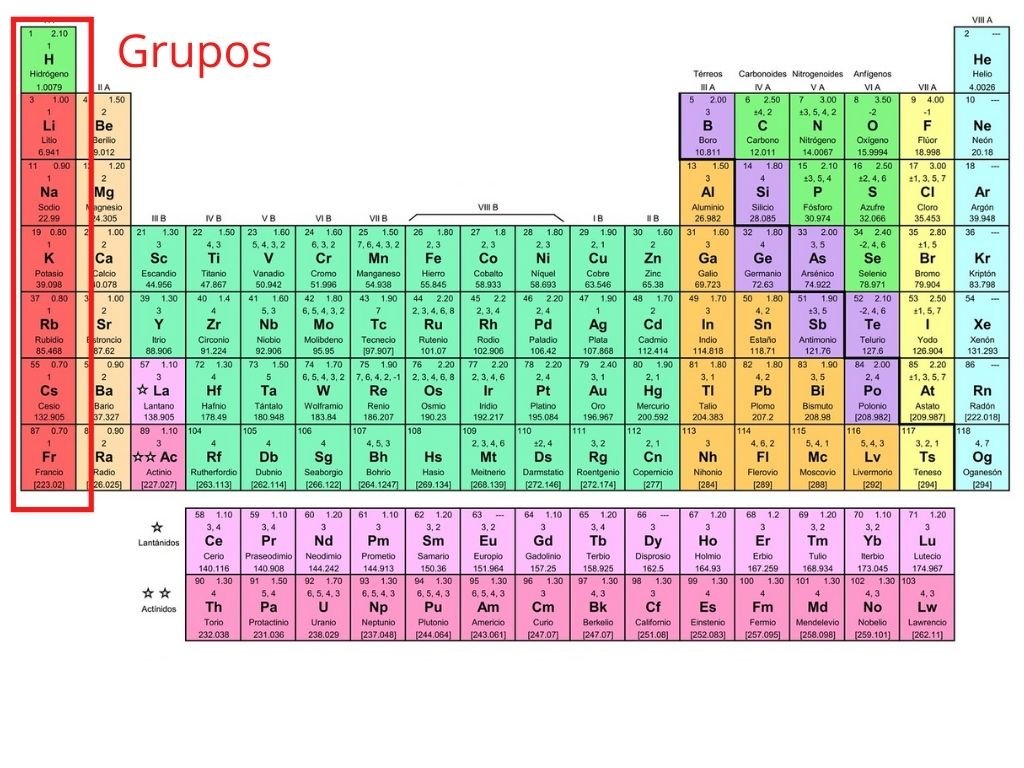
Los elementos químicos que tienen electrones en los orbitales s son los elementos del grupo 1 y del grupo 2 de la tabla periódica. Estos elementos son conocidos como los metales alcalinos y los metales alcalinotérreos, respectivamente. Entre ellos se encuentran el hidrógeno, el litio, el sodio, el potasio, el magnesio, el calcio, el estroncio y el bario.
¿Qué propiedades tienen los elementos que tienen electrones en los orbitales s?
Los elementos que tienen electrones en los orbitales s tienen propiedades similares entre sí. En general, son metales blandos, con baja densidad y punto de fusión bajo. También son altamente reactivos y se oxidan fácilmente en presencia de oxígeno. Además, son buenos conductores de electricidad y calor.
Conclusion
La letra 'S' que aparece en la tabla periódica hace referencia a los orbitales s, que son los más cercanos al núcleo del átomo y tienen forma esférica. Los electrones que se encuentran en estos orbitales tienen la menor cantidad de energía de todos los electrones que se encuentran en los orbitales de un átomo. Los elementos químicos que tienen electrones en los orbitales s tienen propiedades similares entre sí, siendo altamente reactivos y buenos conductores de electricidad y calor.
Preguntas frecuentes
1. ¿Qué es un orbital?
Un orbital es una región del espacio alrededor del núcleo de un átomo donde se puede encontrar un electrón con una alta probabilidad.
2. ¿Qué es la tabla periódica?
La tabla periódica es una herramienta fundamental en la química que muestra los elementos químicos ordenados por su número atómico y su configuración electrónica.
3. ¿Qué es el grupo 1 de la tabla periódica?
El grupo 1 de la tabla periódica está formado por los metales alcalinos, que son elementos altamente reactivos y que tienen un solo electrón en su orbital s exterior.
4. ¿Qué es el grupo 2 de la tabla periódica?
El grupo 2 de la tabla periódica está formado por los metales alcalinotérreos, que son elementos menos reactivos que los metales alcalinos y que tienen dos electrones en su orbital s exterior.
5. ¿Qué es un metal blando?
Un metal blando es un metal que se puede cortar o deformar fácilmente con la presión de los dedos, como el sodio o el potasio.
Deja una respuesta