Aniones y metales: la química de la atracción iónica
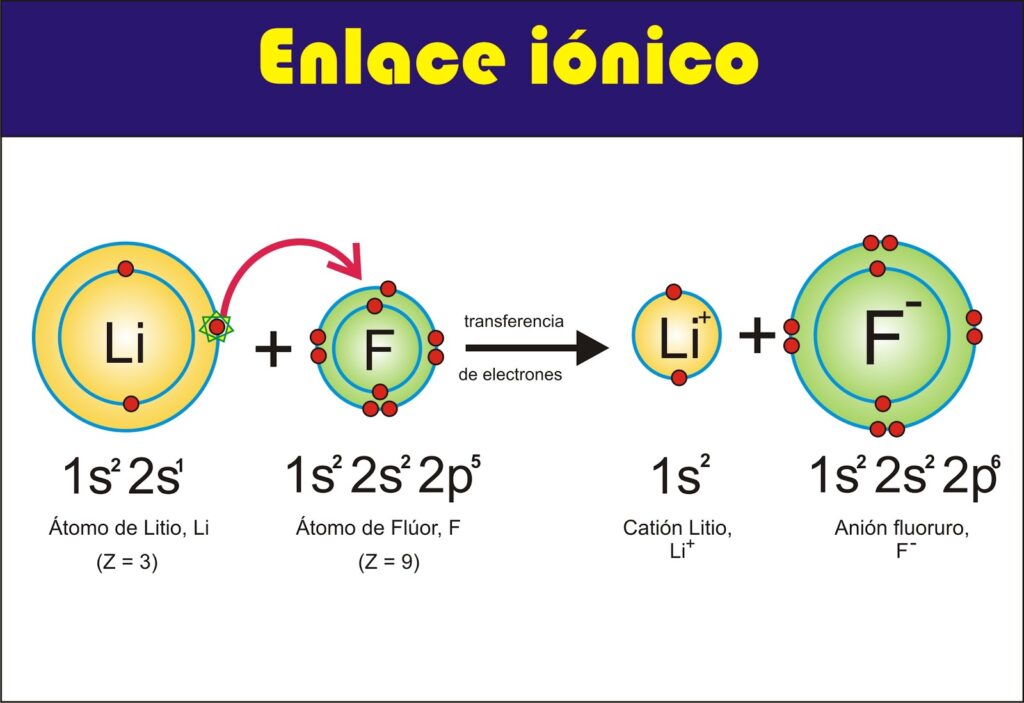
La química es una ciencia fascinante que estudia la composición, estructura y propiedades de la materia. Una de las ramas más interesantes de la química es la química de la atracción iónica, que se refiere a la interacción entre aniones y metales. En este artículo, vamos a explorar la química detrás de esta atracción iónica y cómo se produce.
¿Qué son los aniones y los metales?
Antes de profundizar en la química de la atracción iónica, es importante entender qué son los aniones y los metales. Los aniones son iones con carga negativa, es decir, tienen más electrones que protones. Los metales, por otro lado, son elementos que tienen un brillo característico, son sólidos a temperatura ambiente y son buenos conductores de electricidad y calor.
La atracción iónica
Cuando un anión y un metal interactúan, se produce una atracción iónica. Esto se debe a que los aniones tienen una carga negativa y los metales tienen una carga positiva. La atracción iónica se produce cuando la carga negativa del anión atrae la carga positiva del metal.
Esta atracción iónica es responsable de muchas de las propiedades de los metales. Por ejemplo, la alta conductividad eléctrica y térmica de los metales se debe a la facilidad con la que los electrones pueden moverse a través de los metales debido a la atracción iónica.
La importancia de la atracción iónica
La atracción iónica es un proceso fundamental en la química y tiene importantes aplicaciones en la vida cotidiana. Por ejemplo, la electrónica utiliza la atracción iónica para crear circuitos eléctricos en los que los electrones pueden moverse libremente a través de los metales.
También es importante en la producción de energía. La atracción iónica se utiliza en células solares para producir electricidad a partir de la energía del sol. La atracción iónica también se utiliza en baterías para almacenar energía.
La química detrás de la atracción iónica
La atracción iónica se produce debido a la diferencia de electronegatividad entre el anión y el metal. La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo. Cuando un átomo tiene una alta electronegatividad, atrae electrones con mayor fuerza que otros átomos.
En el caso de los aniones y los metales, los aniones tienen una alta electronegatividad debido a su carga negativa. Los metales, por otro lado, tienen una baja electronegatividad debido a su baja capacidad para atraer electrones.
La diferencia de electronegatividad entre los aniones y los metales crea una atracción iónica. Los aniones atraen electrones del metal, lo que resulta en la formación de una unión iónica. Esta unión iónica es responsable de muchas de las propiedades de los metales, como su alta conductividad eléctrica y térmica.
La química de la oxidación-reducción
La atracción iónica también está relacionada con la química de la oxidación-reducción. La oxidación es la pérdida de electrones por parte de un átomo, mientras que la reducción es la ganancia de electrones por parte de un átomo.
En la atracción iónica, los aniones oxidan los metales al atraer electrones de ellos. Los metales, por otro lado, reducen los aniones al ceder electrones a ellos. Esta transferencia de electrones es responsable de la formación de la unión iónica.
Conclusión
La química de la atracción iónica es fascinante y tiene importantes aplicaciones en la vida cotidiana. La atracción iónica se produce cuando un anión y un metal interactúan debido a la diferencia de electronegatividad entre ellos. Esta atracción iónica es responsable de muchas de las propiedades de los metales, como su alta conductividad eléctrica y térmica.
Preguntas frecuentes
¿Cómo se produce la atracción iónica?
La atracción iónica se produce cuando un anión y un metal interactúan debido a la diferencia de electronegatividad entre ellos. Los aniones tienen una alta electronegatividad debido a su carga negativa, mientras que los metales tienen una baja electronegatividad debido a su baja capacidad para atraer electrones.
¿Qué es la electronegatividad?
La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo.
¿Qué es la oxidación-reducción?
La oxidación es la pérdida de electrones por parte de un átomo, mientras que la reducción es la ganancia de electrones por parte de un átomo.
¿Cuál es la importancia de la atracción iónica?
La atracción iónica es importante en la producción de energía y en la electrónica. También es responsable de muchas de las propiedades de los metales, como su alta conductividad eléctrica y térmica.
¿Cómo se utiliza la atracción iónica en la vida cotidiana?
La atracción iónica se utiliza en la producción de energía y en la electrónica. También se utiliza en la producción de baterías y células solares.
Deja una respuesta