Aumento de la electronegatividad: tabla periódica
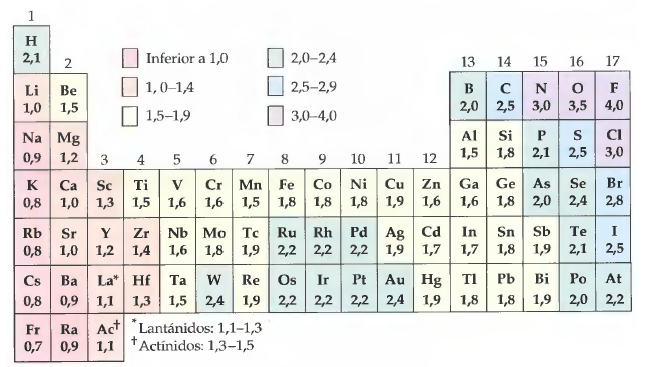
La electronegatividad es una propiedad química que mide la capacidad de un átomo para atraer electrones hacia sí mismo. Esta propiedad es fundamental en la formación de enlaces químicos y en la determinación de la polaridad de las moléculas. En la tabla periódica, la electronegatividad aumenta de izquierda a derecha y de abajo hacia arriba. En este artículo, explicaremos por qué ocurre esto y cómo se puede utilizar esta información en la química.
- ¿Qué es la electronegatividad?
- ¿Por qué aumenta la electronegatividad en la tabla periódica?
- ¿Cómo se utiliza la electronegatividad en la química?
- Conclusión
-
Preguntas frecuentes
- 1. ¿Por qué el flúor tiene la electronegatividad más alta de todos los elementos?
- 2. ¿Por qué la electronegatividad disminuye cuando se avanza hacia abajo en la tabla periódica?
- 3. ¿Cómo se relaciona la electronegatividad con la polaridad de las moléculas?
- 4. ¿Cómo se utiliza la electronegatividad en la predicción de la forma en que se forman los enlaces químicos?
- 5. ¿Por qué se dice que la electronegatividad es una propiedad periódica?
¿Qué es la electronegatividad?
La electronegatividad es una medida de la capacidad de un átomo para atraer electrones hacia su núcleo. Los átomos con mayor electronegatividad tienen una mayor tendencia a atraer electrones y, por lo tanto, a formar enlaces más fuertes con otros átomos. En general, los elementos de la derecha de la tabla periódica tienen una electronegatividad más alta que los elementos de la izquierda.
La electronegatividad se puede medir utilizando varios métodos, pero uno de los más utilizados es la escala de electronegatividad de Pauling. En esta escala, el flúor tiene el valor más alto de electronegatividad (4,0) y el cesio tiene el valor más bajo (0,7).
¿Por qué aumenta la electronegatividad en la tabla periódica?
La electronegatividad aumenta de izquierda a derecha y de abajo hacia arriba en la tabla periódica. Esto se debe a varios factores, entre los que se incluyen:
1. Aumento del número atómico
A medida que se avanza en la tabla periódica de izquierda a derecha, el número atómico de los elementos aumenta. Esto significa que hay más protones en el núcleo del átomo, lo que a su vez significa que hay una mayor carga positiva en el núcleo. Como resultado, los electrones de la capa externa del átomo están más fuertemente atraídos hacia el núcleo, lo que aumenta la electronegatividad del átomo.
2. Tamaño atómico
A medida que se avanza en la tabla periódica de arriba hacia abajo, los átomos se vuelven más grandes. Esto significa que los electrones de la capa externa están más alejados del núcleo, lo que reduce la atracción entre los electrones y el núcleo. Como resultado, la electronegatividad disminuye.
3. Número de capas electrónicas
Los átomos de la derecha de la tabla periódica tienen una capa electrónica externa incompleta, lo que significa que necesitan ganar electrones para completar esta capa. Como resultado, estos átomos tienen una mayor tendencia a atraer electrones hacia sí mismos, lo que aumenta su electronegatividad.
¿Cómo se utiliza la electronegatividad en la química?
La electronegatividad es una propiedad muy importante en la química, ya que determina la forma en que los átomos se unen entre sí para formar moléculas. En general, los átomos con electronegatividades similares tienden a formar enlaces covalentes, mientras que los átomos con electronegatividades muy diferentes tienden a formar enlaces iónicos.
Además, la electronegatividad también es importante en la determinación de la polaridad de las moléculas. Una molécula es polar si tiene una distribución desigual de cargas eléctricas, lo que significa que tiene un polo positivo y un polo negativo. La polaridad de una molécula depende de la diferencia de electronegatividad entre los átomos que la componen.
Conclusión
La electronegatividad es una propiedad fundamental en la química que determina la forma en que los átomos se unen entre sí para formar moléculas. En la tabla periódica, la electronegatividad aumenta de izquierda a derecha y de abajo hacia arriba debido a varios factores, incluyendo el aumento del número atómico, el tamaño atómico y el número de capas electrónicas. La electronegatividad se puede utilizar para predecir la forma en que se forman los enlaces químicos y la polaridad de las moléculas.
Preguntas frecuentes
1. ¿Por qué el flúor tiene la electronegatividad más alta de todos los elementos?
El flúor tiene la electronegatividad más alta debido a su pequeño tamaño atómico y al hecho de que tiene una capa electrónica externa incompleta. Esto significa que tiene una gran tendencia a atraer electrones hacia sí mismo para completar esta capa.
2. ¿Por qué la electronegatividad disminuye cuando se avanza hacia abajo en la tabla periódica?
La electronegatividad disminuye cuando se avanza hacia abajo en la tabla periódica debido al aumento del tamaño atómico. Los electrones de la capa externa están más alejados del núcleo, lo que reduce la atracción entre los electrones y el núcleo.
3. ¿Cómo se relaciona la electronegatividad con la polaridad de las moléculas?
La electronegatividad es importante en la determinación de la polaridad de las moléculas porque la polaridad depende de la diferencia de electronegatividad entre los átomos que la componen. Una molécula es polar si tiene una distribución desigual de cargas eléctricas, lo que significa que tiene un polo positivo y un polo negativo.
4. ¿Cómo se utiliza la electronegatividad en la predicción de la forma en que se forman los enlaces químicos?
La electronegatividad se utiliza para predecir la forma en que se forman los enlaces químicos porque los átomos con electronegatividades similares tienden a formar enlaces covalentes, mientras que los átomos con electronegatividades muy diferentes tienden a formar enlaces iónicos.
5. ¿Por qué se dice que la electronegatividad es una propiedad periódica?
La electronegatividad se considera una propiedad periódica porque aumenta de izquierda a derecha y de abajo hacia arriba en la tabla periódica. Esto significa que hay una tendencia sistemática en la forma en que cambia esta propiedad a medida que se avanza en la tabla periódica.
Deja una respuesta