Descubre cómo identificar electrones en la tabla periódica
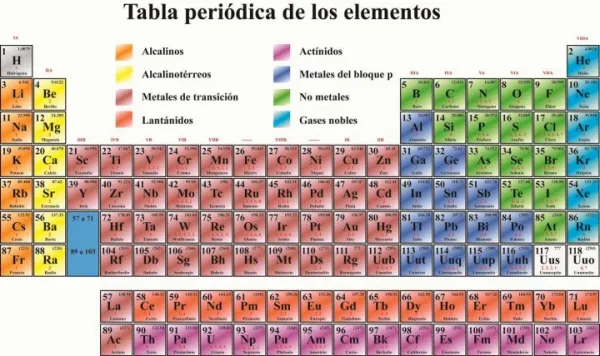
La tabla periódica es una herramienta esencial para los químicos y físicos. Nos proporciona información valiosa sobre los elementos, incluyendo su número atómico, símbolo, masa atómica y configuración electrónica. En este artículo, nos centraremos en cómo identificar electrones en la tabla periódica.
¿Qué son los electrones?
Antes de sumergirnos en cómo identificar electrones en la tabla periódica, es importante tener una comprensión básica de lo que son los electrones. Los electrones son partículas subatómicas con carga negativa que orbitan alrededor del núcleo de un átomo. Son extremadamente pequeños, con una masa aproximadamente 1/1836 de la masa de un protón o un neutrón.
La cantidad de electrones que tiene un átomo determina sus propiedades químicas y su posición en la tabla periódica. Los electrones también son responsables de la mayoría de las reacciones químicas y de la formación de enlaces químicos.
¿Cómo se representa la configuración electrónica?
La configuración electrónica de un átomo se representa utilizando números y letras. El número representa el nivel de energía y la letra representa el tipo de orbital en el que se encuentra el electrón.
Por ejemplo, la configuración electrónica del hidrógeno es 1s1, lo que significa que tiene un electrón en el nivel de energía 1 y en el orbital s.
¿Cómo se identifican los electrones en la tabla periódica?
La tabla periódica está organizada en filas y columnas, y cada elemento tiene su propia configuración electrónica. Al identificar la posición de un elemento en la tabla periódica, podemos determinar su configuración electrónica y, por lo tanto, la cantidad de electrones que tiene.
La posición de un elemento en la tabla periódica también nos proporciona información sobre su reactividad química. Los elementos en la misma columna tienen propiedades químicas similares debido a su configuración electrónica similar.
Identificación de electrones en la tabla periódica por nivel de energía
Los electrones se encuentran en diferentes niveles de energía alrededor del núcleo de un átomo. El nivel de energía más cercano al núcleo es el nivel 1, seguido del nivel 2, luego el nivel 3 y así sucesivamente.
La cantidad máxima de electrones que puede contener un nivel de energía se determina mediante la fórmula 2n^2, donde n es el número del nivel de energía. Por ejemplo, el nivel 1 puede contener un máximo de 2 electrones (2 x 1^2 = 2), el nivel 2 puede contener un máximo de 8 electrones (2 x 2^2 = 8) y el nivel 3 puede contener un máximo de 18 electrones (2 x 3^2 = 18).
Identificación de electrones en la tabla periódica por orbital
Los electrones también se encuentran en diferentes tipos de orbital alrededor del núcleo de un átomo. Los orbitales se denotan por letras, siendo los más comunes s, p, d y f.
Cada orbital puede contener un número máximo de electrones. El orbital s puede contener un máximo de 2 electrones, el orbital p puede contener un máximo de 6 electrones, el orbital d puede contener un máximo de 10 electrones y el orbital f puede contener un máximo de 14 electrones.
Identificación de electrones en la tabla periódica por número atómico
El número atómico de un elemento es el número de protones que tiene en su núcleo. También es igual al número de electrones que tiene, ya que los átomos son eléctricamente neutros.
Al identificar la posición de un elemento en la tabla periódica, podemos determinar su número atómico y, por lo tanto, la cantidad de electrones que tiene.
Conclusión
La identificación de electrones en la tabla periódica es esencial para comprender la química y la física de los elementos. Al conocer la posición de un elemento en la tabla periódica, podemos determinar su configuración electrónica y, por lo tanto, la cantidad de electrones que tiene.
La tabla periódica también nos proporciona información valiosa sobre las propiedades químicas y la reactividad de los elementos.
Preguntas frecuentes
¿Qué es la configuración electrónica?
La configuración electrónica de un átomo se refiere a la distribución de electrones en sus niveles de energía y orbitales.
¿Qué es el número atómico?
El número atómico de un elemento es el número de protones que tiene en su núcleo. También es igual al número de electrones que tiene, ya que los átomos son eléctricamente neutros.
¿Qué es un orbital?
Un orbital es una región del espacio alrededor del núcleo de un átomo en la que es probable encontrar un electrón.
¿Qué es la reactividad química?
La reactividad química se refiere a la capacidad de un elemento para reaccionar con otros elementos y compuestos químicos.
¿Por qué es importante la tabla periódica?
La tabla periódica es una herramienta esencial para los químicos y físicos. Nos proporciona información valiosa sobre los elementos, incluyendo su número atómico, símbolo, masa atómica y configuración electrónica. También nos permite predecir las propiedades químicas y la reactividad de los elementos.
Deja una respuesta