Descubre el avance científico clave detrás del modelo de Thomson
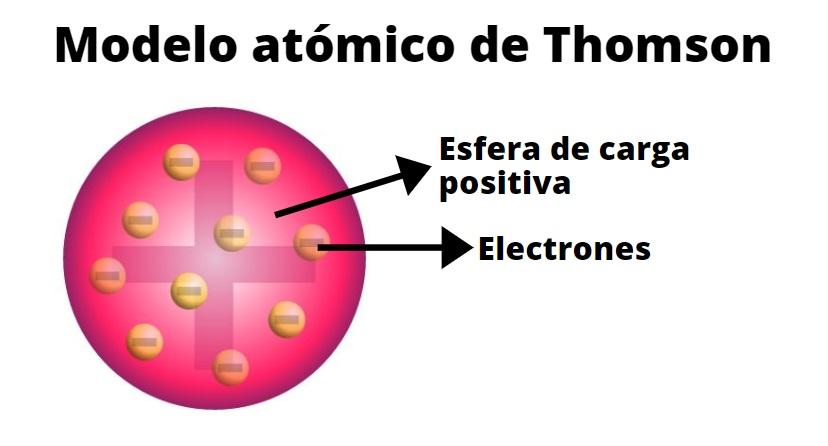
El modelo de Thomson, también conocido como el modelo del pudín de pasas, fue propuesto por el físico británico J.J. Thomson en 1904. Este modelo revolucionó la forma en que los científicos entendían la estructura del átomo, y sentó las bases para el posterior desarrollo de la teoría atómica.
Pero, ¿cuál fue el avance científico clave que hizo posible este modelo? Fue la identificación del electrón como una partícula subatómica separada y distintiva.
Antes del trabajo de Thomson, se creía que el átomo era una esfera sólida e indivisible. Sin embargo, a finales del siglo XIX, varios experimentos demostraron que los átomos tenían una estructura más compleja. Uno de estos experimentos fue el descubrimiento de los rayos catódicos por parte del físico alemán Eugen Goldstein en 1886.
Los rayos catódicos eran corrientes de electrones que fluían a través de un tubo de vacío. Thomson se interesó por estos rayos y comenzó a estudiarlos en detalle. Descubrió que los rayos catódicos eran en realidad corrientes de partículas subatómicas, que más tarde se conocerían como electrones.
Thomson también descubrió que los electrones tenían una carga negativa y una masa muy pequeña, en comparación con la del átomo en su conjunto. Estos hallazgos llevaron a Thomson a proponer que el átomo era como un "pudín" de carga positiva en el que los electrones se encontraban incrustados como "pasas".
Este modelo del átomo fue revolucionario en su época, ya que rompía con la idea de que el átomo era una esfera sólida. Además, el modelo de Thomson explicaba por qué los átomos eran eléctricamente neutros, a pesar de tener partículas con cargas positivas y negativas.
El modelo de Thomson también sentó las bases para el posterior desarrollo de la teoría atómica. En 1911, el físico neozelandés Ernest Rutherford llevó a cabo un experimento en el que bombardeó una lámina de oro con partículas alfa. Los resultados de este experimento demostraron que la mayor parte del átomo era espacio vacío, y que la carga positiva y la masa del átomo estaban concentradas en un núcleo central.
Este descubrimiento llevó a la propuesta de un nuevo modelo del átomo por parte de Rutherford, en el que los electrones orbitaban alrededor del núcleo central. Este modelo fue el precursor del modelo actual del átomo, en el que los electrones se distribuyen en capas alrededor del núcleo.
El avance científico clave detrás del modelo de Thomson fue la identificación del electrón como una partícula subatómica separada y distintiva. Este descubrimiento permitió a Thomson proponer un nuevo modelo del átomo, que revolucionó la forma en que los científicos entendían la estructura del átomo en ese momento. El modelo de Thomson sentó las bases para el posterior desarrollo de la teoría atómica y sigue siendo un hito importante en la historia de la ciencia.
Preguntas frecuentes
¿Qué son los rayos catódicos?
Los rayos catódicos son corrientes de electrones que fluyen a través de un tubo de vacío. Fueron descubiertos por el físico alemán Eugen Goldstein en 1886.
¿Por qué el modelo de Thomson fue importante?
El modelo de Thomson fue importante porque revolucionó la forma en que los científicos entendían la estructura del átomo. Antes del trabajo de Thomson, se creía que el átomo era una esfera sólida e indivisible. El modelo de Thomson propuso que el átomo era como un "pudín" de carga positiva en el que los electrones se encontraban incrustados como "pasas". Este modelo sentó las bases para el posterior desarrollo de la teoría atómica.
¿Cómo se descubrieron los electrones?
Los electrones fueron descubiertos por J.J. Thomson en sus estudios de los rayos catódicos en la década de 1890. Thomson descubrió que los rayos catódicos eran en realidad corrientes de partículas subatómicas, que más tarde se conocerían como electrones.
¿Qué es el modelo actual del átomo?
El modelo actual del átomo es un modelo en el que los electrones se distribuyen en capas alrededor del núcleo. En este modelo, el núcleo central está compuesto por protones y neutrones, y los electrones se distribuyen en orbitales alrededor del núcleo.
¿Quién propuso el modelo del átomo con un núcleo central?
El modelo del átomo con un núcleo central fue propuesto por el físico neozelandés Ernest Rutherford en 1911. Rutherford llevó a cabo un experimento en el que bombardeó una lámina de oro con partículas alfa, lo que le permitió descubrir que la mayor parte del átomo era espacio vacío, y que la carga positiva y la masa del átomo estaban concentradas en un núcleo central.
Deja una respuesta