Descubre el misterio de la Z en la tabla periódica
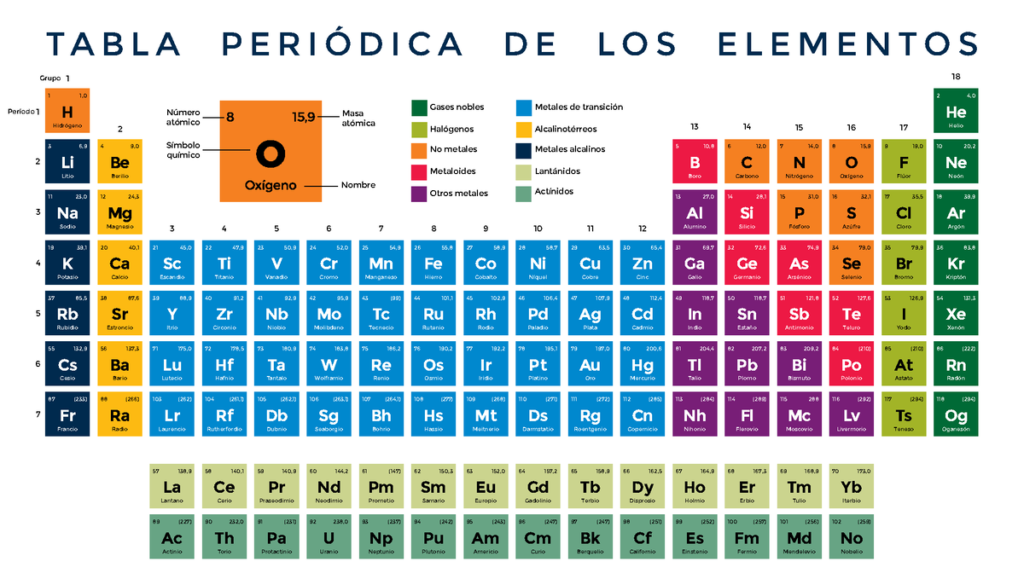
La tabla periódica es una herramienta fundamental en la química, ya que permite organizar los elementos de acuerdo a sus propiedades físicas y químicas. Cada elemento se representa por un símbolo, que incluye una letra o una combinación de letras. Sin embargo, algunos elementos tienen una letra en su símbolo que no es muy conocida: la Z. En este artículo, descubriremos el misterio de la Z en la tabla periódica.
¿Qué es la Z en la tabla periódica?
La Z en la tabla periódica se refiere al número atómico de un elemento. El número atómico es el número de protones en el núcleo de un átomo, lo que significa que determina la identidad del elemento. Por lo tanto, la Z es un número entero que se utiliza para identificar un elemento de manera única.
¿Por qué es importante la Z en la tabla periódica?
El número atómico es una propiedad fundamental de un elemento, ya que determina el número de electrones en un átomo en estado neutro y, por lo tanto, sus propiedades químicas. Por ejemplo, el hidrógeno y el helio tienen un número atómico de 1 y 2, respectivamente, lo que significa que tienen un electrón y dos electrones, respectivamente. Esta diferencia en el número de electrones es lo que determina que el hidrógeno sea altamente reactivo y el helio sea un gas noble no reactivo.
Además, la Z también se utiliza para determinar la posición de un elemento en la tabla periódica. Los elementos se organizan en filas y columnas de acuerdo a su número atómico, lo que permite predecir sus propiedades y comportamiento químico.
¿Cómo se representa la Z en la tabla periódica?
La Z se representa en la tabla periódica como un número entero en la esquina superior izquierda de cada cuadro de elemento. Por ejemplo, el carbono tiene un número atómico de 6, lo que significa que su símbolo es C y su Z es 6.
¿Hay algún elemento con una Z mayor a 118?
Actualmente, se han descubierto y confirmado 118 elementos, y cada uno tiene un número atómico único que va desde 1 hasta 118. Sin embargo, se han teorizado la existencia de elementos con números atómicos mayores, pero aún no se han descubierto.
¿Hay alguna relación entre la Z y la masa atómica de un elemento?
La masa atómica de un elemento es la suma de los protones y neutrones en su núcleo. Aunque la masa atómica está relacionada con la Z, no es lo mismo. Por ejemplo, el carbono tiene seis protones y seis neutrones en su núcleo, lo que significa que su masa atómica es de aproximadamente 12. Sin embargo, hay isotopos del carbono con una masa atómica diferente debido a la variación en el número de neutrones.
Conclusión
La Z en la tabla periódica es una propiedad fundamental de los elementos, ya que se utiliza para identificarlos de manera única y determinar su posición en la tabla periódica. Aunque es posible que no sea tan conocida como otras letras en los símbolos de los elementos, la Z es esencial para comprender la química y la física de los elementos.
Preguntas frecuentes
- ¿Qué significa el número atómico de un elemento?
- ¿Por qué es importante la Z en la tabla periódica?
- ¿Cómo se representa la Z en la tabla periódica?
- ¿Hay algún elemento con una Z mayor a 118?
- ¿Hay alguna relación entre la Z y la masa atómica de un elemento?
Deja una respuesta