Descubre el orden de los elementos en la tabla periódica
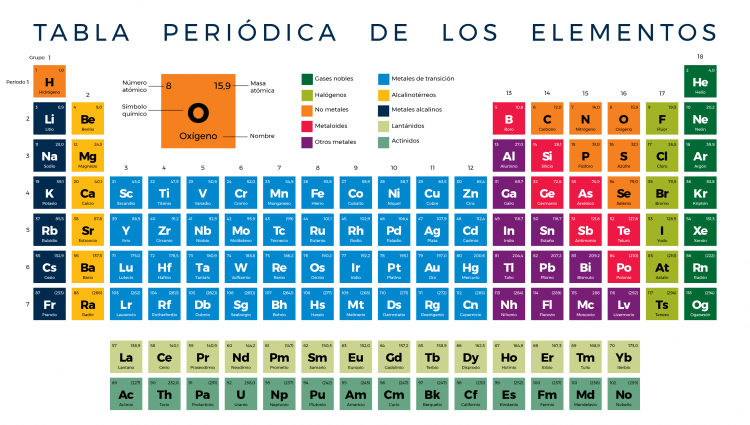
La tabla periódica es una herramienta fundamental en la química y otras ciencias relacionadas. Contiene información valiosa sobre los elementos, incluyendo su número atómico, configuración electrónica, propiedades físicas y químicas, y más. Pero, ¿alguna vez te has preguntado cómo se ordenan los elementos en la tabla periódica? En este artículo, exploraremos el orden de los elementos y cómo se relacionan entre sí.
La organización de la tabla periódica
La tabla periódica se organiza en filas horizontales llamadas períodos y columnas verticales llamadas grupos. Los elementos en cada fila tienen el mismo número de orbitales electrónicos, mientras que los elementos en cada columna tienen configuraciones electrónicas similares. El número atómico, que es el número de protones en el núcleo de un átomo, aumenta de izquierda a derecha en cada fila.
Grupos y bloques
Los grupos en la tabla periódica se numeran del 1 al 18, y cada uno tiene un nombre o símbolo. Los dos grupos más importantes son el grupo 1, también conocido como los metales alcalinos, y el grupo 18, también conocido como los gases nobles. Los elementos en cada grupo tienen propiedades químicas y físicas similares debido a su configuración electrónica.
Además, la tabla periódica se divide en bloques que corresponden a los subniveles de energía de los electrones. Los bloques se designan con letras: s, p, d y f. Los bloques s y p son los más comunes y contienen la mayoría de los elementos conocidos.
Períodos
Los períodos son las filas horizontales en la tabla periódica y están numerados del 1 al 7. Los elementos en cada período tienen el mismo número de orbitales electrónicos. El período 1 solo tiene dos elementos, hidrógeno y helio, mientras que el período 2 tiene ocho elementos, el período 3 tiene 18 y así sucesivamente.
El orden de los elementos en la tabla periódica
Los elementos se ordenan en la tabla periódica según su número atómico. El elemento más ligero, hidrógeno, tiene un número atómico de 1 y se encuentra en la esquina superior izquierda de la tabla periódica. Los elementos se ordenan progresivamente hacia la derecha y hacia abajo de la tabla periódica, con el elemento más pesado, oganesón, con un número atómico de 118, en la esquina inferior derecha.
Configuración electrónica
La configuración electrónica de un elemento se refiere a la distribución de electrones en los niveles de energía. Cada electrón se asigna a un nivel de energía y a un subnivel (s, p, d o f) dentro de ese nivel de energía. Los electrones se llenan en orden creciente de energía, comenzando con el nivel de energía más bajo.
La configuración electrónica de un elemento se puede representar de diferentes maneras, como la notación de configuración electrónica abreviada o la notación de configuración electrónica completa. La notación abreviada utiliza la configuración de gas noble anterior al elemento para abreviar la configuración electrónica.
Propiedades de los elementos
Las propiedades de los elementos se relacionan con su posición en la tabla periódica. Los elementos en el mismo grupo tienen propiedades químicas y físicas similares debido a su configuración electrónica. Por ejemplo, los metales alcalinos (grupo 1) son altamente reactivos debido a su configuración electrónica externa, mientras que los gases nobles (grupo 18) son extremadamente estables debido a su configuración electrónica completa.
Además, las propiedades físicas, como el punto de fusión, el punto de ebullición y la densidad, también varían de acuerdo con la posición del elemento en la tabla periódica.
Conclusión
La tabla periódica es una herramienta indispensable en la química y otras ciencias relacionadas. La organización de la tabla periódica se basa en el número atómico y la configuración electrónica de los elementos. Los elementos se ordenan en filas horizontales llamadas períodos y columnas verticales llamadas grupos. Los elementos en cada grupo tienen propiedades químicas y físicas similares debido a su configuración electrónica.
Preguntas frecuentes
1. ¿Por qué se llama tabla periódica?
Se llama tabla periódica porque los elementos se organizan en períodos y grupos, y las propiedades de los elementos varían periódicamente según su posición en la tabla.
2. ¿Cuál es el elemento más pesado en la tabla periódica?
El elemento más pesado en la tabla periódica es el oganesón, con un número atómico de 118.
3. ¿Por qué los elementos en el mismo grupo tienen propiedades similares?
Los elementos en el mismo grupo tienen propiedades similares debido a su configuración electrónica. Los elementos en el mismo grupo tienen la misma cantidad de electrones en su capa externa, lo que les da propiedades químicas y físicas similares.
4. ¿Qué es la configuración electrónica?
La configuración electrónica de un elemento se refiere a la distribución de electrones en los niveles de energía. Cada electrón se asigna a un nivel de energía y a un subnivel (s, p, d o f) dentro de ese nivel de energía.
5. ¿Por qué la tabla periódica es importante en la química?
La tabla periódica es importante en la química porque proporciona información sobre los elementos, su configuración electrónica, sus propiedades químicas y físicas y más. La tabla periódica es una herramienta fundamental para comprender la química y otras ciencias relacionadas.
Deja una respuesta