Descubre el orden secreto detrás de la tabla periódica
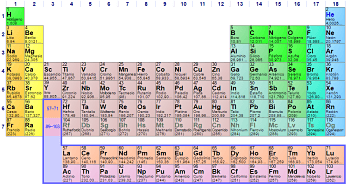
La tabla periódica es uno de los logros más importantes de la química y la ciencia en general. Es una herramienta indispensable para los químicos, ya que les permite conocer las propiedades de los elementos y cómo se relacionan entre sí. Pero, ¿alguna vez te has preguntado cómo se organizan los elementos en la tabla periódica? ¿Por qué algunos elementos están juntos y otros están separados por varios espacios?
En este artículo, te explicaremos el orden secreto detrás de la tabla periódica, cómo se organizan los elementos y por qué es tan importante entender su estructura.
La historia de la tabla periódica
La tabla periódica fue creada por Dmitry Mendeleev en 1869. Mendeleev fue un químico ruso que estaba tratando de organizar los elementos conocidos en ese momento. Descubrió que los elementos se podían ordenar por su peso atómico, y que los elementos con propiedades similares se repetían en intervalos regulares.
Mendeleev organizó los elementos en filas y columnas, y dejó espacios en blanco para elementos que aún no habían sido descubiertos. Sus predicciones fueron tan precisas que cuando se descubrieron nuevos elementos, sus propiedades coincidían exactamente con lo que había predicho.
Con el tiempo, la tabla periódica se ha refinado y ampliado, y ahora incluye más de 100 elementos.
La estructura de la tabla periódica
La tabla periódica se organiza en filas horizontales llamadas periodos y columnas verticales llamadas grupos. Los elementos en cada fila tienen el mismo número de capas electrónicas, y los elementos en cada columna tienen el mismo número de electrones en su capa más externa.
Los elementos en la tabla periódica se organizan de acuerdo a su número atómico, que es la cantidad de protones en el núcleo de un átomo. El número atómico también determina la posición del elemento en la tabla periódica.
Los grupos de la tabla periódica
La tabla periódica se divide en 18 grupos, cada uno con su propia designación y características. Algunos de los grupos más importantes son:
Grupo 1: Los metales alcalinos
Los metales alcalinos son los elementos en la primera columna de la tabla periódica. Tienen un solo electrón en su capa más externa y son altamente reactivos. Los metales alcalinos incluyen el litio, el sodio y el potasio.
Grupo 2: Los metales alcalinotérreos
Los metales alcalinotérreos son los elementos en la segunda columna de la tabla periódica. Tienen dos electrones en su capa más externa y son menos reactivos que los metales alcalinos. Los metales alcalinotérreos incluyen el calcio, el magnesio y el bario.
Grupo 17: Los halógenos
Los halógenos son los elementos en la séptima columna de la tabla periódica. Tienen siete electrones en su capa más externa y son altamente reactivos. Los halógenos incluyen el cloro, el flúor y el yodo.
Grupo 18: Los gases nobles
Los gases nobles son los elementos en la octava columna de la tabla periódica. Tienen una capa electrónica completa y son muy estables. Los gases nobles incluyen el helio, el neón y el argón.
Los periodos de la tabla periódica
La tabla periódica también se divide en siete periodos, cada uno con elementos que tienen el mismo número de capas electrónicas. Los elementos en cada periodo tienen propiedades químicas similares debido a su configuración electrónica.
La importancia de la tabla periódica
La tabla periódica es una herramienta invaluable para los químicos y científicos en todo el mundo. Les permite predecir cómo los elementos reaccionarán y se combinan, y les da una comprensión más profunda de la estructura de la materia.
La comprensión de la tabla periódica también es esencial para la industria y la tecnología, ya que muchos materiales y productos se basan en las propiedades de los elementos.
Conclusión
La tabla periódica es una herramienta fundamental para la química y la ciencia en general. Su estructura organizada nos permite comprender mejor los elementos y cómo interactúan entre sí. Al comprender la tabla periódica, podemos hacer predicciones precisas sobre las propiedades de los elementos y usar esta información para mejorar la tecnología y la industria.
Preguntas frecuentes
1. ¿Por qué se llama tabla periódica?
La tabla periódica se llama así porque los elementos se organizan en períodos, que se repiten periódicamente.
2. ¿Qué son los elementos transicionales?
Los elementos transicionales son los elementos en las secciones centrales de la tabla periódica, que incluyen metales como el hierro, el cobre y el oro.
3. ¿Qué es la electronegatividad?
La electronegatividad es la medida de la capacidad de un átomo para atraer electrones hacia sí mismo en una molécula. Los elementos con alta electronegatividad atraen electrones con fuerza, mientras que los elementos con baja electronegatividad tienden a ceder electrones.
4. ¿Por qué algunos elementos están separados por varios espacios en la tabla periódica?
Los elementos están separados por varios espacios en la tabla periódica debido a la necesidad de mantener elementos con propiedades químicas similares en la misma columna.
5. ¿Cuál es el elemento más pesado en la tabla periódica?
El elemento más pesado en la tabla periódica es el oganesón, que tiene un número atómico de 118.
Deja una respuesta