Descubre el proceso de formación de productos en reacciones químicas
Las reacciones químicas son procesos fundamentales en la química y en la vida cotidiana. En ellas, se transforman sustancias, llamadas reactivos, en otras, llamadas productos. En este artículo, descubrirás el proceso de formación de productos en reacciones químicas.
¿Qué son las reacciones químicas?
Las reacciones químicas son procesos en los que los átomos, iones o moléculas de una o varias sustancias (los reactivos) se transforman en otras sustancias (los productos) a través de la ruptura y formación de enlaces químicos.
¿Cómo se representan las reacciones químicas?
Las reacciones químicas se representan mediante ecuaciones químicas, en las que se escriben los nombres o fórmulas de los reactivos y los productos, separados por una flecha que indica la dirección de la reacción.
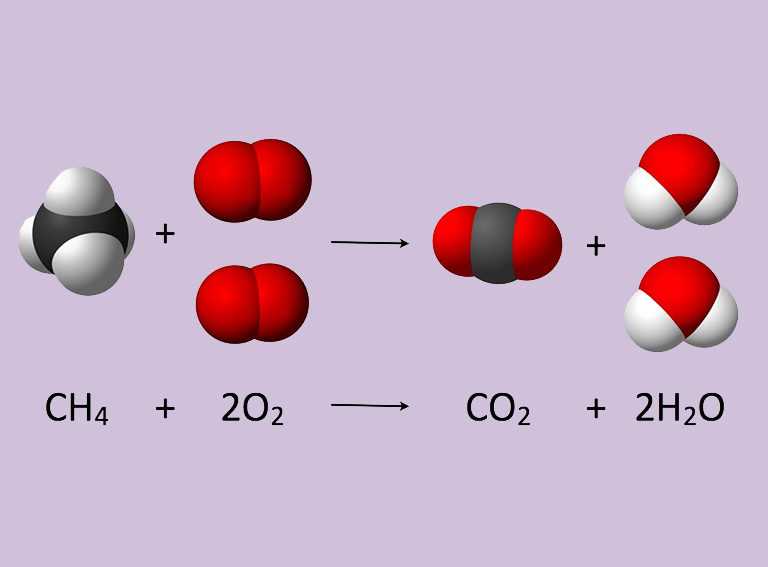
Por ejemplo, la reacción de combustión del metano (CH4) con oxígeno (O2) para producir dióxido de carbono (CO2) y agua (H2O) se representa de la siguiente manera:
CH4 + 2O2 → CO2 + 2H2O
¿Cómo se lleva a cabo una reacción química?
Para que una reacción química ocurra, es necesario que los reactivos entren en contacto y se colisionen con suficiente energía para romper los enlaces químicos y formar nuevos enlaces.
La energía necesaria para que una reacción química ocurra se llama energía de activación. Esta energía puede ser proporcionada por diferentes factores, como la temperatura, la presión o la luz.
¿Qué factores influyen en una reacción química?
Las reacciones químicas pueden ser influenciadas por diferentes factores, como la concentración de los reactivos, la temperatura, la presión y la presencia de catalizadores.
Por ejemplo, si aumentamos la concentración de los reactivos en una reacción, aumentamos la probabilidad de colisiones entre ellos y, por lo tanto, la velocidad de la reacción.
¿Qué tipos de reacciones químicas existen?
Existen diferentes tipos de reacciones químicas, como las de síntesis, en las que dos o más sustancias se combinan para formar un producto; las de descomposición, en las que una sustancia se rompe en dos o más productos; y las de sustitución, en las que un átomo o grupo de átomos de una sustancia es reemplazado por otro átomo o grupo de átomos.
¿Qué es la ley de conservación de la masa?
La ley de conservación de la masa establece que en una reacción química, la masa total de los reactivos es igual a la masa total de los productos. Esto significa que la materia no se crea ni se destruye, solo se transforma.
Por lo tanto, al balancear una ecuación química, es necesario asegurarse de que la cantidad de átomos de cada elemento sea la misma en ambos lados de la ecuación.
Conclusión
Las reacciones químicas son procesos fundamentales en la química y en la vida cotidiana. En ellas, se transforman sustancias mediante la ruptura y formación de enlaces químicos. Para que una reacción química ocurra, es necesario que los reactivos entren en contacto y se colisionen con suficiente energía para romper los enlaces químicos y formar nuevos enlaces. Existen diferentes tipos de reacciones químicas, como las de síntesis, descomposición y sustitución. Además, la ley de conservación de la masa establece que en una reacción química, la masa total de los reactivos es igual a la masa total de los productos.
Preguntas frecuentes
¿Qué es un reactivo?
Un reactivo es una sustancia que participa en una reacción química y se transforma en otra sustancia llamada producto.
¿Qué es un producto?
Un producto es una sustancia que se forma en una reacción química a partir de los reactivos.
¿Qué es la energía de activación?
La energía de activación es la energía necesaria para que una reacción química ocurra. Esta energía puede ser proporcionada por diferentes factores, como la temperatura, la presión o la luz.
¿Qué es un catalizador?
Un catalizador es una sustancia que aumenta la velocidad de una reacción química sin ser consumido en la reacción.
¿Por qué es importante balancear una ecuación química?
Es importante balancear una ecuación química para asegurarse de que la cantidad de átomos de cada elemento sea la misma en ambos lados de la ecuación y cumplir con la ley de conservación de la masa.
Deja una respuesta