Descubre la estructura del átomo y sus partículas subatómicas
Desde la antigüedad, el ser humano ha tenido curiosidad por entender el mundo que le rodea y ha tratado de explicar los fenómenos que observa en su día a día. Uno de los grandes descubrimientos de la ciencia moderna ha sido el de la estructura del átomo y sus partículas subatómicas. En este artículo, te explicaremos qué es un átomo, cuáles son sus componentes y cómo se organizan.
¿Qué es un átomo?
Un átomo es la unidad más pequeña de un elemento químico que mantiene sus propiedades. Está formado por un núcleo central, que contiene protones y neutrones, y por electrones que giran alrededor del núcleo. El núcleo es la parte más densa del átomo y los electrones se encuentran en la zona más externa.
Partículas subatómicas
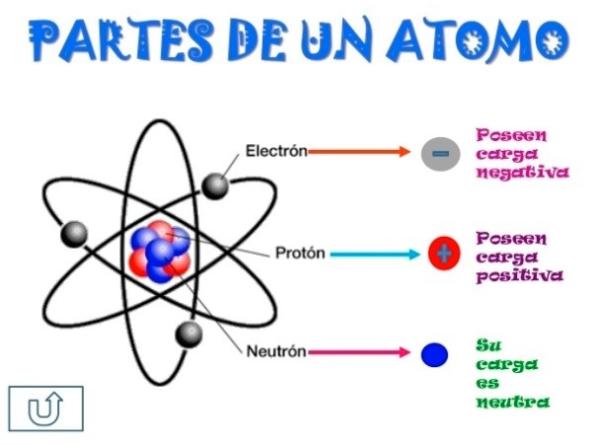
El átomo está compuesto por tres partículas subatómicas: protones, neutrones y electrones. Cada una de ellas tiene una carga eléctrica específica y una masa distinta.
Protones
Los protones son partículas con carga positiva que se encuentran en el núcleo del átomo. La carga eléctrica de un protón es igual y opuesta a la del electrón. Es decir, si el electrón tiene una carga negativa, el protón tiene una carga positiva. La masa de un protón es aproximadamente igual a la de un neutrón.
Neutrones
Los neutrones son partículas sin carga eléctrica que también se encuentran en el núcleo del átomo. La masa de un neutrón es aproximadamente igual a la de un protón. La presencia de neutrones en el núcleo de un átomo es lo que define su isótopo.
Electrones
Los electrones son partículas con carga negativa que giran alrededor del núcleo en órbitas específicas. La masa de un electrón es mucho menor que la de un protón o un neutrón. Los electrones son los responsables de los enlaces químicos entre átomos y de las reacciones químicas que se producen en los elementos.
Organización del átomo
La organización del átomo se basa en la distribución de las partículas subatómicas en el núcleo y en las órbitas de los electrones. El número de protones en el núcleo de un átomo determina su número atómico y su lugar en la tabla periódica de los elementos.
La distribución de los electrones en las órbitas se rige por el modelo atómico de Bohr. Según este modelo, los electrones se organizan en distintas capas o niveles de energía, que se denominan K, L, M, N, O, P y Q. La capa K es la más cercana al núcleo y la que tiene menos energía, mientras que la capa Q es la más lejana y la que tiene más energía.
Conclusiones
El átomo es la unidad básica de la materia y está compuesto por protones, neutrones y electrones. Cada una de estas partículas tiene una carga eléctrica específica y una masa distinta. La organización del átomo se basa en la distribución de estas partículas en el núcleo y en las órbitas de los electrones. Entender la estructura del átomo es fundamental para comprender las propiedades y reacciones químicas de los elementos.
Preguntas frecuentes
¿Qué es un átomo?
Un átomo es la unidad más pequeña de un elemento químico que mantiene sus propiedades. Está formado por un núcleo central, que contiene protones y neutrones, y por electrones que giran alrededor del núcleo.
¿Cuáles son las partículas subatómicas?
Las partículas subatómicas son protones, neutrones y electrones.
¿Qué es el número atómico?
El número atómico es el número de protones que hay en el núcleo de un átomo. Determina el lugar del átomo en la tabla periódica de los elementos.
¿Qué es un isótopo?
Un isótopo es un átomo que tiene el mismo número de protones pero un número diferente de neutrones en su núcleo.
¿Qué es el modelo atómico de Bohr?
El modelo atómico de Bohr es una representación del átomo en la que los electrones se organizan en distintas capas o niveles de energía alrededor del núcleo.
Deja una respuesta