Descubre la ubicación en la tabla periódica de 1s2 2s2 2p6 3s2 3p
La tabla periódica es una herramienta fundamental en la química, ya que nos permite conocer la ubicación de cada elemento y, por lo tanto, entender sus propiedades y comportamientos. Una de las formas de representar la ubicación de un elemento en la tabla periódica es a través de su configuración electrónica, que nos muestra cómo están distribuidos los electrones en los distintos niveles y subniveles de energía.
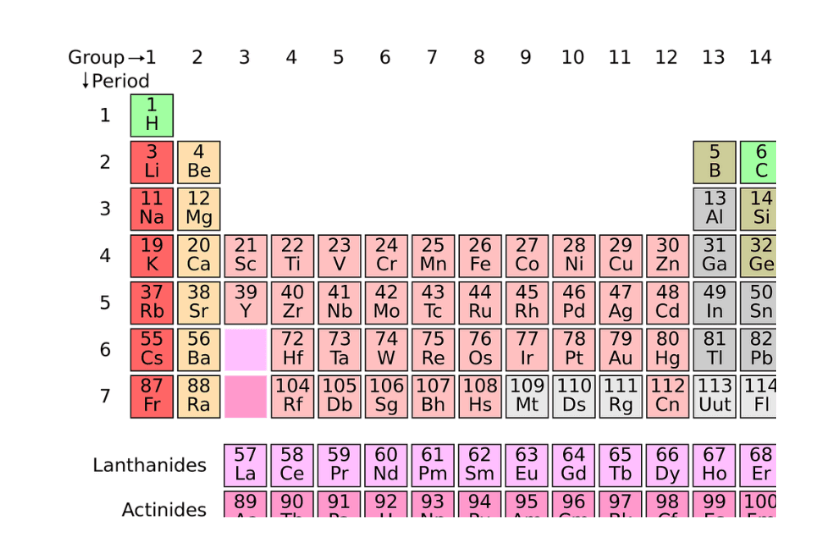
La configuración electrónica 1s2 2s2 2p6 3s2 3p corresponde al átomo de Silicio (Si), que se encuentra en el tercer período y el grupo 14 de la tabla periódica. Para entender mejor su ubicación, es importante conocer algunos conceptos básicos sobre la tabla periódica.
- ¿Qué es la tabla periódica?
- ¿Cómo se lee una configuración electrónica?
- ¿Qué son los niveles y subniveles de energía?
- ¿Qué significa la configuración electrónica del Silicio?
- ¿Por qué el Silicio se encuentra en el grupo 14 de la tabla periódica?
- ¿Por qué es importante conocer la ubicación de los elementos en la tabla periódica?
- Conclusión
- Preguntas frecuentes
¿Qué es la tabla periódica?
La tabla periódica es una disposición ordenada de los elementos químicos, en la que cada elemento se representa por su símbolo y se organiza en filas y columnas según sus propiedades químicas y físicas. Esta disposición permite predecir las propiedades de los elementos que aún no han sido descubiertos y entender las relaciones entre los elementos existentes.
¿Cómo se lee una configuración electrónica?
Una configuración electrónica se lee de la siguiente manera: se indica el número del nivel de energía (1, 2, 3, etc.), seguido de la letra del subnivel (s, p, d, f) y el número de electrones que tiene ese subnivel. Por ejemplo, la configuración electrónica del hidrógeno es 1s1, lo que significa que tiene un electrón en el subnivel 1s.
¿Qué son los niveles y subniveles de energía?
Los electrones en un átomo se distribuyen en distintos niveles de energía, que se representan por números enteros (1, 2, 3, etc.). Cada nivel de energía tiene uno o más subniveles, que se representan por letras (s, p, d, f) y que corresponden a distintas formas de movimiento de los electrones. El subnivel s tiene forma esférica y puede contener hasta 2 electrones, mientras que los subniveles p, d y f tienen formas más complejas y pueden contener hasta 6, 10 y 14 electrones, respectivamente.
¿Qué significa la configuración electrónica del Silicio?
La configuración electrónica del Silicio es 1s2 2s2 2p6 3s2 3p. Esto significa que el Silicio tiene dos electrones en el nivel 1, dos electrones en el subnivel s del nivel 2, seis electrones en el subnivel p del nivel 2, dos electrones en el subnivel s del nivel 3 y dos electrones en el subnivel p del nivel 3.
¿Por qué el Silicio se encuentra en el grupo 14 de la tabla periódica?
El grupo 14 de la tabla periódica es conocido como el grupo del Carbono, porque el Carbono es el elemento más representativo de este grupo. Los elementos de este grupo tienen en común que tienen cuatro electrones en su subnivel externo (subnivel p del nivel 3), lo que les permite formar cuatro enlaces covalentes y, por lo tanto, tener una gran variedad de compuestos.
El Silicio se encuentra en el grupo 14 porque tiene la misma configuración electrónica externa que los demás elementos de este grupo: 2 electrones en el subnivel s del nivel 3 y 2 electrones en el subnivel p del nivel 3.
¿Por qué es importante conocer la ubicación de los elementos en la tabla periódica?
Conocer la ubicación de los elementos en la tabla periódica es fundamental para entender sus propiedades y comportamientos. La ubicación de un elemento nos indica su configuración electrónica, su número atómico, su masa atómica, su valencia y su reactividad, entre otras características. Además, la tabla periódica nos permite predecir las propiedades de los elementos que aún no han sido descubiertos y diseñar nuevos materiales y compuestos.
Conclusión
La configuración electrónica 1s2 2s2 2p6 3s2 3p corresponde al átomo de Silicio, que se encuentra en el tercer período y el grupo 14 de la tabla periódica. Conocer la ubicación de un elemento en la tabla periódica es fundamental para entender sus propiedades y comportamientos, y la configuración electrónica es una forma útil de representar esta ubicación.
Preguntas frecuentes
¿Qué significa la configuración electrónica del átomo?
La configuración electrónica del átomo es una representación de cómo están distribuidos los electrones en los distintos niveles y subniveles de energía.
¿Qué son los niveles y subniveles de energía?
Los niveles y subniveles de energía son las distintas capas de energía en las que se distribuyen los electrones en un átomo.
¿Qué es el grupo 14 de la tabla periódica?
El grupo 14 de la tabla periódica es un grupo de elementos que tienen cuatro electrones en su subnivel externo y que comparten ciertas propiedades químicas y físicas.
¿Qué información nos da la tabla periódica?
La tabla periódica nos da información sobre la ubicación, configuración electrónica, número atómico, masa atómica, valencia y reactividad de los elementos químicos.
¿Por qué es importante conocer la ubicación de los elementos en la tabla periódica?
Conocer la ubicación de los elementos en la tabla periódica es importante para entender sus propiedades y comportamientos, y para poder diseñar nuevos materiales y compuestos.
Deja una respuesta