Descubre los metales alcalinos de la tabla periódica
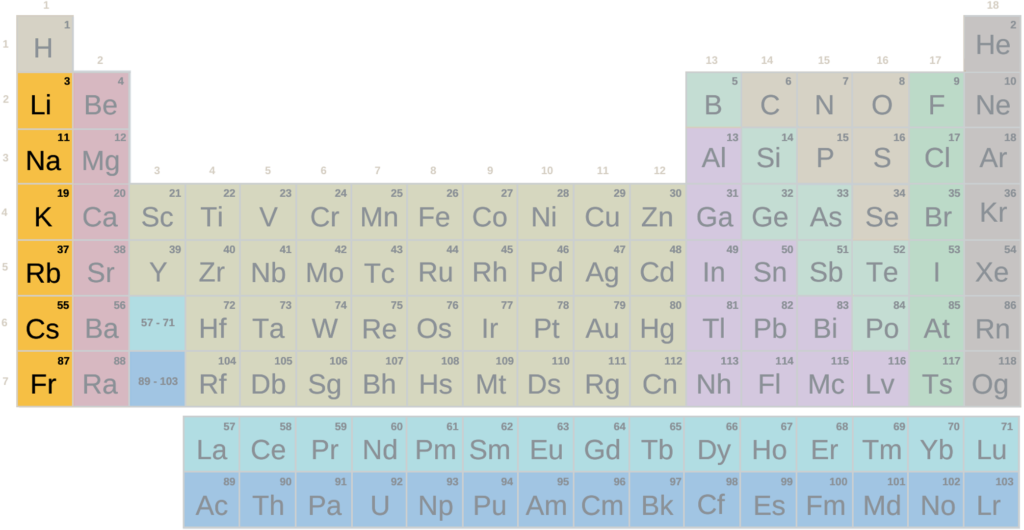
La tabla periódica es una herramienta fundamental en la química, ya que permite clasificar los elementos según su estructura atómica y propiedades químicas. Una de las categorías de elementos que se pueden encontrar en la tabla periódica son los metales alcalinos, los cuales se encuentran en el grupo 1 y son conocidos por su gran reactividad química y su capacidad para formar iones con carga positiva. En este artículo, vamos a descubrir más acerca de los metales alcalinos y su importancia en la química.
¿Qué son los metales alcalinos?
Los metales alcalinos son aquellos que se encuentran en el grupo 1 de la tabla periódica y se caracterizan por tener un solo electrón en su capa externa. Los elementos que pertenecen a esta categoría son: Litio (Li), Sodio (Na), Potasio (K), Rubidio (Rb), Cesio (Cs) y Francio (Fr). Todos estos elementos tienen propiedades químicas similares, como una baja densidad, un bajo punto de fusión y ebullición, y una gran reactividad.
Propiedades químicas de los metales alcalinos
Los metales alcalinos son altamente reactivos debido a su estructura atómica. Al tener un solo electrón en su capa externa, estos elementos tienen una gran tendencia a perder ese electrón y formar un ion con carga positiva. Como resultado, los metales alcalinos son altamente electropositivos y reaccionan con facilidad con otros elementos para formar compuestos iónicos.
Además de su gran reactividad, los metales alcalinos también tienen una baja densidad y un bajo punto de fusión y ebullición. Esto se debe a que los enlaces metálicos que mantienen unidos los átomos de estos elementos son muy débiles, lo que significa que se rompen fácilmente cuando se aplica calor o se aplica presión.
Usos de los metales alcalinos
Los metales alcalinos tienen una amplia variedad de usos en la industria y en la vida cotidiana. Por ejemplo, el litio se utiliza en la fabricación de baterías recargables y en la producción de aleaciones ligeras. El sodio se utiliza en la producción de vidrio, en la fabricación de productos químicos y en la purificación de metales. El potasio se utiliza en la producción de fertilizantes y en la fabricación de jabones y detergentes.
Tabla de propiedades físicas y químicas de los metales alcalinos
| Elemento | Símbolo | Número atómico | Punto de fusión (°C) | Punto de ebullición (°C) | Densidad (g/cm³) |
|---------|--------|----------------|----------------------|------------------------|------------------|
| Litio | Li | 3 | 180.5 | 1,342 | 0.534 |
| Sodio | Na | 11 | 97.8 | 883 | 0.971 |
| Potasio | K | 19 | 63.38 | 759 | 0.862 |
| Rubidio | Rb | 37 | 38.89 | 686 | 1.532 |
| Cesio | Cs | 55 | 28.44 | 671 | 1.93 |
| Francio | Fr | 87 | 27 | 677 | - |
Curiosidades sobre los metales alcalinos
- El sodio es uno de los elementos más abundantes en la corteza terrestre.
- El potasio es esencial para el funcionamiento del cuerpo humano, ya que ayuda a regular el equilibrio de fluidos y la función muscular.
- El rubidio y el cesio son elementos raros y se utilizan en la investigación científica para estudiar los efectos de la radiación en los seres vivos.
- El francio es el elemento más raro y menos estable de los metales alcalinos. Es tan reactivo que se descompone rápidamente en otros elementos.
Conclusión
Los metales alcalinos son una categoría de elementos de la tabla periódica que se caracterizan por su gran reactividad química y sus propiedades físicas y químicas únicas. Estos elementos tienen una amplia variedad de usos en la industria y en la vida cotidiana, y son esenciales para la investigación científica en muchos campos. Si bien los metales alcalinos pueden ser peligrosos en ciertas situaciones, su importancia en la química y en la vida humana es innegable.
Preguntas frecuentes
¿Por qué los metales alcalinos son tan reactivos?
Los metales alcalinos son reactivos porque tienen un solo electrón en su capa externa, lo que significa que tienen una gran tendencia a perder ese electrón y formar un ion con carga positiva. Como resultado, estos elementos reaccionan con facilidad con otros elementos para formar compuestos iónicos.
¿Cómo se utilizan los metales alcalinos en la vida cotidiana?
Los metales alcalinos se utilizan en una amplia variedad de productos de uso cotidiano, como baterías recargables, jabones y detergentes, productos químicos y fertilizantes.
¿Por qué el potasio es esencial para el cuerpo humano?
El potasio es esencial para el cuerpo humano porque ayuda a regular el equilibrio de fluidos y la función muscular. También es necesario para mantener una presión arterial saludable y para el correcto funcionamiento del sistema nervioso.
¿Qué es el francio y por qué es tan raro?
El francio es el elemento más raro y menos estable de los metales alcalinos. Se encuentra en pequeñas cantidades en la corteza terrestre y es extremadamente reactivo, lo que significa que se descompone rápidamente en otros elementos. Debido a su rareza y alta reactividad, el francio se utiliza principalmente en la investigación científica.
¿Cuáles son los elementos más comunes en los metales alcalinos?
El sodio y el potasio son los elementos más comunes en los metales alcalinos debido a su abundancia en la corteza terrestre. Sin embargo, el litio también se utiliza ampliamente en la producción de baterías recargables y aleaciones ligeras.
Deja una respuesta