Descubre los metales de transición en la tabla periódica
¿Alguna vez has oído hablar de los metales de transición en la tabla periódica? Si no es así, no te preocupes, en este artículo te explicaremos todo lo que necesitas saber sobre ellos.
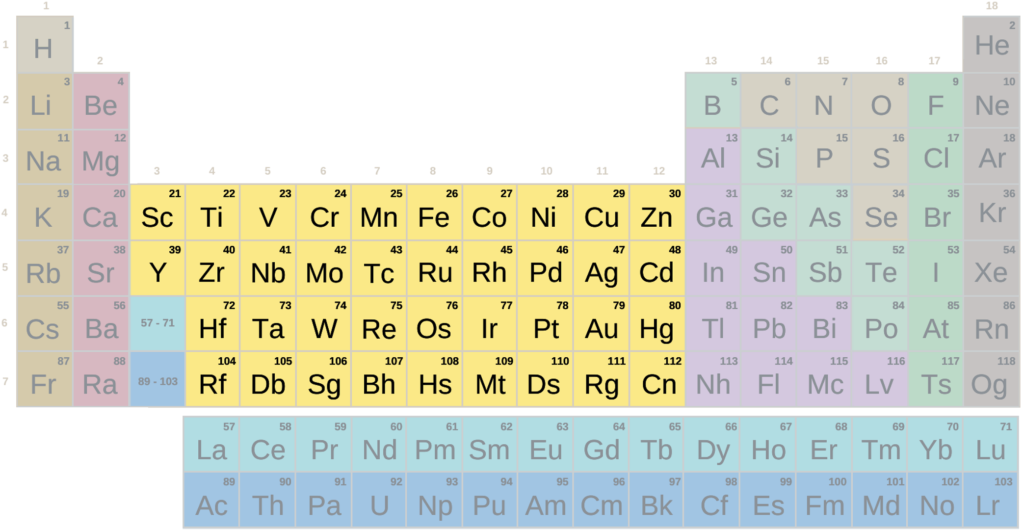
Los metales de transición son un grupo de elementos químicos que se encuentran en la tabla periódica entre los grupos 3 y 12. Estos elementos tienen en común su capacidad para formar múltiples estados de oxidación, lo que significa que pueden unirse a otros átomos de diversas maneras y crear diversas combinaciones químicas.
¿Qué son los metales de transición?
Los metales de transición son aquellos que se encuentran en la parte central de la tabla periódica. Estos elementos tienen una configuración electrónica que les permite formar enlaces químicos fuertes y estables, lo que los convierte en elementos muy importantes para la química y la física.
Características de los metales de transición
Los metales de transición tienen varias características que los distinguen de otros elementos. Algunas de estas características incluyen:
- Múltiples estados de oxidación: los metales de transición pueden formar múltiples estados de oxidación, lo que les permite unirse a otros átomos de diversas maneras y crear diversas combinaciones químicas.
- Conductividad: los metales de transición son excelentes conductores de electricidad y calor.
- Dureza: muchos metales de transición son muy duros y resistentes a la deformación.
- Coloración: algunos metales de transición tienen una coloración distintiva, como el cobre rojo o el oro amarillo.
Ejemplos de metales de transición
Entre los metales de transición más comunes se encuentran:
- Hierro (Fe)
- Cobre (Cu)
- Níquel (Ni)
- Cinc (Zn)
- Plata (Ag)
- Oro (Au)
Importancia de los metales de transición
Los metales de transición son elementos muy importantes para la química y la física. Estos elementos se utilizan en una amplia variedad de aplicaciones, desde la fabricación de objetos cotidianos hasta la investigación científica.
Algunas de las aplicaciones más comunes de los metales de transición incluyen:
- Fabricación de joyas y objetos decorativos: los metales de transición como el oro y la plata se utilizan comúnmente en la fabricación de joyas y objetos decorativos debido a su coloración distintiva y su alta resistencia a la corrosión.
- Fabricación de herramientas y maquinaria: muchos metales de transición, como el hierro y el cobre, se utilizan en la fabricación de herramientas y maquinaria debido a su dureza y resistencia a la deformación.
- Electrónica: los metales de transición son excelentes conductores de electricidad, lo que los convierte en elementos clave para la fabricación de dispositivos electrónicos, como ordenadores y teléfonos móviles.
- Investigación científica: los metales de transición se utilizan en la investigación científica para estudiar las propiedades químicas y físicas de los elementos y para desarrollar nuevos materiales y tecnologías.
Conclusión
Los metales de transición son un grupo importante de elementos químicos que se encuentran en la tabla periódica entre los grupos 3 y 12. Estos elementos tienen en común su capacidad para formar múltiples estados de oxidación y su importancia en la química, la física y la fabricación de objetos cotidianos. Si alguna vez te preguntas por qué algunos metales tienen una coloración distintiva o por qué ciertos objetos son tan resistentes, es posible que la respuesta se encuentre en los metales de transición.
Preguntas frecuentes
¿Qué es un estado de oxidación?
Un estado de oxidación es una medida de la capacidad de un átomo para perder o ganar electrones en un enlace químico. Los metales de transición tienen la capacidad de formar múltiples estados de oxidación, lo que les permite unirse a otros átomos de diversas maneras y crear diversas combinaciones químicas.
¿Por qué los metales de transición son tan importantes?
Los metales de transición son importantes porque tienen una configuración electrónica que les permite formar enlaces químicos fuertes y estables. Estos elementos se utilizan en una amplia variedad de aplicaciones, desde la fabricación de joyas y objetos decorativos hasta la investigación científica.
¿Todos los metales son metales de transición?
No, no todos los metales son metales de transición. Los metales de transición se encuentran en la parte central de la tabla periódica, entre los grupos 3 y 12. Otros metales, como el aluminio y el calcio, se encuentran en otros lugares de la tabla periódica y tienen propiedades diferentes.
¿Qué es la conductividad?
La conductividad es la capacidad de un material para conducir electricidad o calor. Los metales de transición son excelentes conductores de electricidad y calor, lo que los convierte en elementos clave para la fabricación de dispositivos electrónicos y herramientas y maquinaria.
¿Cómo se utilizan los metales de transición en la investigación científica?
Los metales de transición se utilizan en la investigación científica para estudiar las propiedades químicas y físicas de los elementos y para desarrollar nuevos materiales y tecnologías. Estos elementos son importantes para la química y la física debido a su capacidad para formar múltiples estados de oxidación y su capacidad para formar enlaces químicos fuertes y estables.
Deja una respuesta