Descubre los nombres de las familias de la tabla periódica
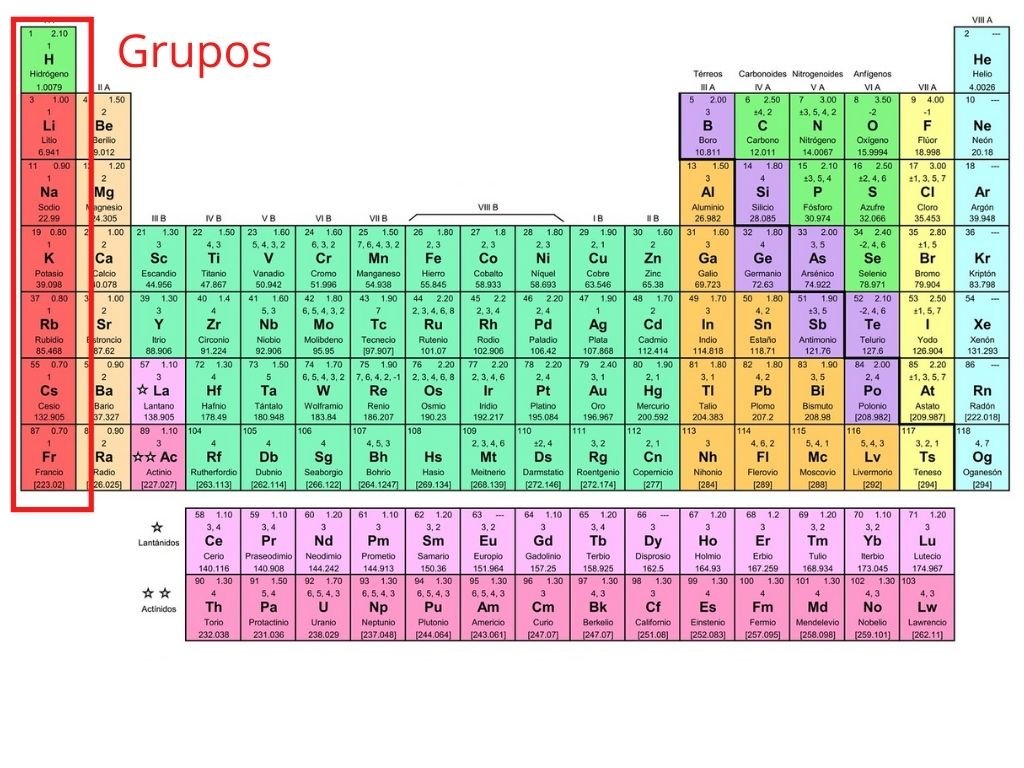
La tabla periódica es una herramienta fundamental en el estudio de la química. En ella se encuentran todos los elementos químicos conocidos hasta la fecha, organizados en filas y columnas según sus propiedades físicas y químicas. Una de las formas en que los elementos están agrupados es en familias o grupos, según sus características comunes. En este artículo, descubrirás los nombres de las familias de la tabla periódica y algunas de sus propiedades.
Familia 1: Metales alcalinos
Los metales alcalinos son los elementos que se encuentran en la primera columna de la tabla periódica. Estos elementos son altamente reactivos y tienen un solo electrón en su capa externa, lo que los hace muy propensos a formar compuestos. Los metales alcalinos incluyen el litio, el sodio, el potasio, el rubidio, el cesio y el francio.
Propiedades de los metales alcalinos:
- Son altamente reactivos
- Son blandos y maleables
- Tienen un bajo punto de fusión
- Son buenos conductores de calor y electricidad
- Forman compuestos iónicos con no metales.
Familia 2: Metales alcalinotérreos
Los metales alcalinotérreos son los elementos que se encuentran en la segunda columna de la tabla periódica. Estos elementos tienen dos electrones en su capa externa y son menos reactivos que los metales alcalinos. Algunos ejemplos de metales alcalinotérreos son el calcio, el magnesio y el bario.
Propiedades de los metales alcalinotérreos:
- Son menos reactivos que los metales alcalinos
- Tienen un punto de fusión más alto que los metales alcalinos
- Son buenos conductores de calor y electricidad
- Forman compuestos iónicos con no metales.
Familia 3: Metales de transición
Los metales de transición son los elementos que se encuentran en las columnas 3 a 12 de la tabla periódica. Estos elementos tienen una gran variedad de propiedades y se utilizan en una amplia variedad de aplicaciones, desde la joyería hasta la construcción de automóviles. Algunos ejemplos de metales de transición son el hierro, el cobre, el oro y el platino.
Propiedades de los metales de transición:
- Tienen alta conductividad térmica y eléctrica
- Son maleables y dúctiles
- Tienen puntos de fusión y ebullición altos
- Forman compuestos iónicos y covalentes.
Familia 4: Carbonoideos
Los carbonoideos son los elementos que se encuentran en la columna 14 de la tabla periódica. Estos elementos tienen cuatro electrones en su capa externa y son conocidos por su capacidad para formar enlaces covalentes. El carbono, el silicio y el germanio son algunos ejemplos de carbonoideos.
Propiedades de los carbonoideos:
- Tienen una gran capacidad para formar enlaces covalentes
- Tienen puntos de fusión y ebullición altos
- Tienen una gran variedad de propiedades, desde conductores hasta aislantes.
Familia 5: Nitrogenoideos
Los nitrogenoideos son los elementos que se encuentran en la columna 15 de la tabla periódica. Estos elementos tienen cinco electrones en su capa externa y son conocidos por su capacidad para formar compuestos con nitrógeno. El nitrógeno, el fósforo y el arsénico son algunos ejemplos de nitrogenoideos.
Propiedades de los nitrogenoideos:
- Tienen una gran capacidad para formar compuestos con nitrógeno
- Tienen puntos de fusión y ebullición moderados
- Tienen propiedades semiconductoras.
Familia 6: Calcógenos
Los calcógenos son los elementos que se encuentran en la columna 16 de la tabla periódica. Estos elementos tienen seis electrones en su capa externa y son conocidos por su capacidad para formar compuestos con oxígeno. El oxígeno, el azufre y el selenio son algunos ejemplos de calcógenos.
Propiedades de los calcógenos:
- Tienen una gran capacidad para formar compuestos con oxígeno
- Tienen puntos de fusión y ebullición moderados
- Tienen propiedades semiconductoras.
Familia 7: Halógenos
Los halógenos son los elementos que se encuentran en la columna 17 de la tabla periódica. Estos elementos tienen siete electrones en su capa externa y son altamente reactivos. El fluoruro, el cloro, el bromo y el yodo son algunos ejemplos de halógenos.
Propiedades de los halógenos:
- Son altamente reactivos
- Tienen puntos de fusión y ebullición bajos
- Son tóxicos.
Familia 8: Gases nobles
Los gases nobles son los elementos que se encuentran en la columna 18 de la tabla periódica. Estos elementos tienen una capa externa completa y son conocidos por su estabilidad y falta de reactividad. El helio, el neón, el argón, el criptón, el xenón y el radón son algunos ejemplos de gases nobles.
Propiedades de los gases nobles:
- Son estables y no reactivos
- Tienen puntos de fusión y ebullición bajos
- Son utilizados en lámparas y dispositivos de iluminación.
Conclusión
La tabla periódica es una herramienta fundamental en la química y la ciencia en general. Las familias de la tabla periódica son una forma de agrupar los elementos según sus características comunes. Cada familia tiene sus propias propiedades y aplicaciones únicas en la industria y la tecnología.
Preguntas frecuentes
1. ¿Cuántas familias hay en la tabla periódica?
Hay ocho familias en la tabla periódica.
2. ¿Qué es un metal alcalino?
Un metal alcalino es un elemento altamente reactivo que se encuentra en la primera columna de la tabla periódica.
3. ¿Qué es un gas noble?
Un gas noble es un elemento que se encuentra en la columna 18 de la tabla periódica y es conocido por su estabilidad y falta de reactividad.
4. ¿Qué es un carbonoideo?
Un carbonoideo es un elemento que se encuentra en la columna 14 de la tabla periódica y tiene cuatro electrones en su capa externa.
5. ¿Qué es un halógeno?
Un halógeno es un elemento altamente reactivo que se encuentra en la columna 17 de la tabla periód
Deja una respuesta