Enlaces covalentes: descubre sus propiedades físicas y químicas
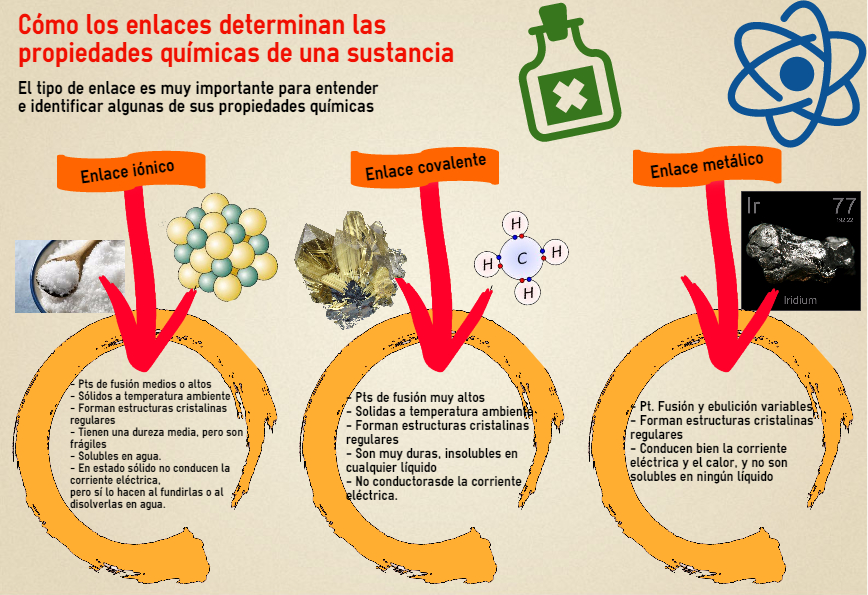
Los enlaces covalentes son aquellos enlaces químicos en los que dos átomos comparten electrones para formar una molécula. Estos enlaces son esenciales para la formación de compuestos orgánicos e inorgánicos, y tienen propiedades físicas y químicas únicas que hacen que sean esenciales para la vida tal como la conocemos.
En este artículo, vamos a explorar las propiedades físicas y químicas de los enlaces covalentes, así como sus aplicaciones en la vida cotidiana.
Propiedades físicas de los enlaces covalentes
Los enlaces covalentes tienen un punto de fusión y un punto de ebullición relativamente bajos en comparación con los enlaces iónicos. Esto se debe a que los enlaces covalentes no tienen una carga eléctrica neta y, por lo tanto, no producen atracciones electrostáticas fuertes entre las moléculas. En cambio, los enlaces covalentes son mantenidos unidos por fuerzas intermoleculares más débiles, como las fuerzas de Van der Waals.
Los enlaces covalentes también tienden a tener una baja conductividad eléctrica y térmica. Esto se debe a que los electrones compartidos están "atrapados" entre los átomos y no pueden moverse libremente a través de la molécula. Como resultado, los enlaces covalentes no pueden conducir bien la electricidad o el calor.
Propiedades químicas de los enlaces covalentes
Los enlaces covalentes son muy estables y no reaccionan fácilmente con otros compuestos químicos. Sin embargo, algunos enlaces covalentes pueden ser más polares que otros, lo que significa que los electrones compartidos no están distribuidos uniformemente entre los átomos.
Cuando un enlace covalente es polar, los átomos que comparten los electrones tendrán cargas parciales positivas o negativas. Esto puede hacer que la molécula sea atraída o repelida por otras moléculas con cargas opuestas, lo que puede influir en su reactividad química.
Aplicaciones de los enlaces covalentes
Los enlaces covalentes se encuentran en una gran variedad de compuestos, desde las proteínas y los carbohidratos hasta los plásticos y los medicamentos. La capacidad de los átomos para compartir electrones y formar enlaces covalentes es lo que permite que se formen moléculas complejas.
En la industria, los enlaces covalentes se utilizan para fabricar materiales sintéticos, como los plásticos y las fibras textiles. También se utilizan en la fabricación de medicamentos y productos farmacéuticos, donde los enlaces covalentes pueden proporcionar una mayor estabilidad y durabilidad.
Conclusiones
Los enlaces covalentes son esenciales para la formación de compuestos químicos y tienen propiedades físicas y químicas únicas. Su capacidad para compartir electrones y formar moléculas complejas es lo que permite la vida tal como la conocemos. Los enlaces covalentes se encuentran en una gran variedad de compuestos, desde los carbohidratos y las proteínas hasta los plásticos y los medicamentos.
Preguntas frecuentes
1. ¿Qué es un enlace covalente?
Un enlace covalente es un enlace químico en el que dos átomos comparten electrones para formar una molécula.
2. ¿Cuáles son las propiedades físicas de los enlaces covalentes?
Los enlaces covalentes tienen un punto de fusión y un punto de ebullición relativamente bajos en comparación con los enlaces iónicos. También tienden a tener una baja conductividad eléctrica y térmica.
3. ¿Cuáles son las propiedades químicas de los enlaces covalentes?
Los enlaces covalentes son muy estables y no reaccionan fácilmente con otros compuestos químicos. Sin embargo, algunos enlaces covalentes pueden ser más polares que otros, lo que significa que los electrones compartidos no están distribuidos uniformemente entre los átomos.
4. ¿Dónde se encuentran los enlaces covalentes?
Los enlaces covalentes se encuentran en una gran variedad de compuestos, desde los carbohidratos y las proteínas hasta los plásticos y los medicamentos.
5. ¿Cuáles son las aplicaciones de los enlaces covalentes?
Los enlaces covalentes se utilizan en la fabricación de materiales sintéticos, como los plásticos y las fibras textiles, así como en la fabricación de medicamentos y productos farmacéuticos.
Deja una respuesta