Enlaces covalentes polares: ¿Qué son y cómo se forman?
Los enlaces covalentes son aquellos enlaces químicos que se forman cuando dos átomos comparten electrones. En los enlaces covalentes polares, los electrones compartidos se encuentran más cerca de uno de los átomos que del otro. Esto da como resultado una distribución de carga desigual en la molécula, lo que la convierte en una molécula polar.
Para entender mejor cómo se forman los enlaces covalentes polares, es necesario conocer un poco sobre la electronegatividad. La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo. Los átomos con mayor electronegatividad tienen una mayor capacidad para atraer electrones, mientras que los átomos con menor electronegatividad tienen una menor capacidad para hacerlo.
Cuando dos átomos con electronegatividades diferentes se unen para formar un enlace covalente, los electrones compartidos se encuentran más cerca del átomo con mayor electronegatividad. Esto se debe a que este átomo ejerce una mayor atracción sobre los electrones compartidos. Como resultado, la carga se distribuye de manera desigual en la molécula, lo que la convierte en una molécula polar.
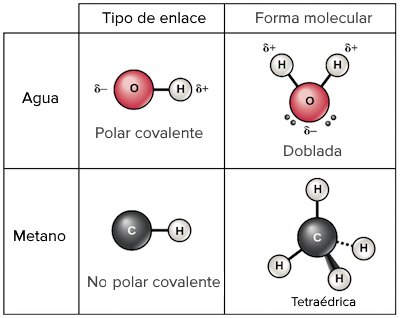
Un ejemplo común de enlace covalente polar es el agua. El oxígeno tiene una mayor electronegatividad que el hidrógeno, por lo que los electrones compartidos se encuentran más cerca del oxígeno. Esto da como resultado una distribución de carga desigual en la molécula, con el oxígeno ligeramente cargado negativamente y los hidrógenos ligeramente cargados positivamente.
Los enlaces covalentes polares se forman cuando dos átomos con electronegatividades diferentes se unen para compartir electrones. Esto da como resultado una distribución de carga desigual en la molécula, lo que la convierte en una molécula polar.
- ¿Cómo se diferencian los enlaces covalentes polares de los no polares?
- ¿Por qué es importante entender los enlaces covalentes polares?
- ¿Cómo afecta la polaridad de una molécula a su comportamiento en soluciones?
- ¿Cómo se puede determinar la polaridad de una molécula?
- ¿Qué aplicaciones tienen los enlaces covalentes polares?
¿Cómo se diferencian los enlaces covalentes polares de los no polares?
Los enlaces covalentes no polares son aquellos en los que los electrones compartidos se encuentran igualmente cerca de ambos átomos. Esto da como resultado una molécula no polar, ya que la carga se distribuye de manera uniforme en la molécula. Los enlaces covalentes polares, por otro lado, tienen una distribución de carga desigual en la molécula, lo que la convierte en una molécula polar.
¿Por qué es importante entender los enlaces covalentes polares?
Comprender los enlaces covalentes polares es importante porque nos ayuda a entender las propiedades físicas y químicas de las moléculas. Las moléculas polares tienen propiedades diferentes a las moléculas no polares. Por ejemplo, las moléculas polares son solubles en agua, mientras que las moléculas no polares no lo son. También tienen diferentes puntos de ebullición y fusión.
¿Cómo afecta la polaridad de una molécula a su comportamiento en soluciones?
La polaridad de una molécula afecta su capacidad para disolverse en soluciones. Las moléculas polares se disuelven fácilmente en soluciones polares, como el agua, debido a las fuerzas de atracción entre las cargas opuestas. Las moléculas no polares, por otro lado, no se disuelven fácilmente en soluciones polares debido a la falta de atracción entre las cargas.
¿Cómo se puede determinar la polaridad de una molécula?
La polaridad de una molécula se puede determinar examinando la geometría de la molécula y la electronegatividad de los átomos que la componen. Si la molécula tiene una geometría simétrica y todos los átomos tienen la misma electronegatividad, entonces la molécula será no polar. Si la molécula tiene una geometría asimétrica y los átomos tienen diferentes electronegatividades, entonces la molécula será polar.
¿Qué aplicaciones tienen los enlaces covalentes polares?
Los enlaces covalentes polares tienen muchas aplicaciones en la vida cotidiana. Por ejemplo, la polaridad del agua permite que sea un buen disolvente para muchas sustancias, lo que la convierte en una parte esencial de la vida en la Tierra. También es importante en la separación de compuestos en la industria química y en la producción de medicamentos y productos farmacéuticos. Además, la polaridad de las moléculas también es importante en la interacción entre las biomoléculas en los organismos vivos.
Deja una respuesta