Equilibrio eléctrico: átomos neutros con carga equilibrada
¿Qué es el equilibrio eléctrico?
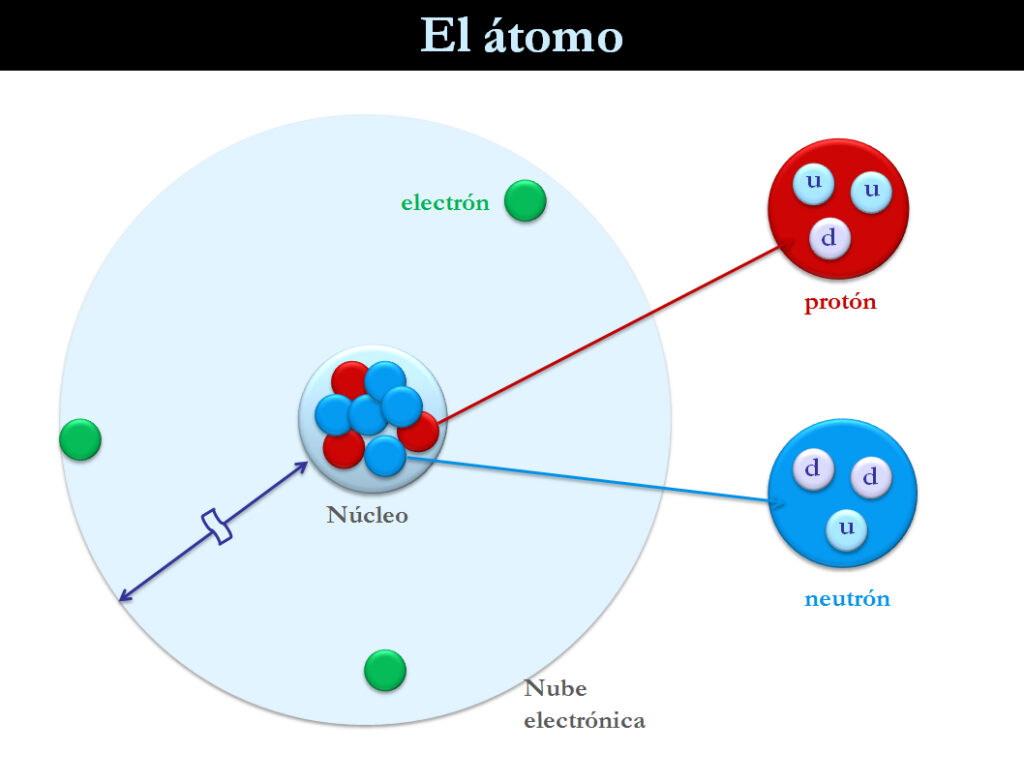
El equilibrio eléctrico es un estado en el que los átomos tienen una carga equilibrada en su interior, lo que significa que tienen el mismo número de electrones que de protones. Los átomos son las unidades básicas de la materia y están compuestos por protones, electrones y neutrones. Los protones tienen carga positiva, los electrones tienen carga negativa y los neutrones no tienen carga.
Cuando los átomos tienen una carga equilibrada, están en un estado de equilibrio eléctrico. Esto significa que no hay un exceso de carga eléctrica en el átomo y que no atrae o repele a otros átomos o moléculas cargados eléctricamente.
¿Cómo se logra el equilibrio eléctrico?
El equilibrio eléctrico se logra cuando un átomo tiene el mismo número de electrones que de protones. Los electrones se encuentran en la capa externa de los átomos, mientras que los protones están en el núcleo del átomo.
Cuando dos átomos se unen para formar una molécula, los electrones de la capa externa se comparten entre los átomos. Si ambos átomos tienen el mismo número de electrones y protones, entonces la molécula resultante tendrá una carga equilibrada.
Importancia del equilibrio eléctrico
El equilibrio eléctrico es importante para la estabilidad de los átomos y moléculas en la naturaleza. Si un átomo tiene una carga desequilibrada, puede atraer o repeler a otros átomos o moléculas cargados eléctricamente. Esto puede causar reacciones químicas no deseadas o incluso explosiones.
Además, el equilibrio eléctrico es fundamental para el funcionamiento de los circuitos eléctricos y electrónicos. Si un circuito tiene una carga desequilibrada, puede causar cortocircuitos o fallos en el sistema.
Cómo se mide el equilibrio eléctrico
El equilibrio eléctrico se puede medir a través del potencial de ionización y la electronegatividad de los átomos. El potencial de ionización es la energía necesaria para quitar un electrón de un átomo, mientras que la electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo.
Los átomos con baja electronegatividad y alto potencial de ionización tienen una carga equilibrada y son menos propensos a reaccionar químicamente con otros átomos y moléculas.
Ejemplos de átomos con carga equilibrada
Algunos ejemplos de átomos con carga equilibrada son el hidrógeno, el helio, el litio, el berilio, el boro, el carbono, el nitrógeno, el oxígeno, el flúor, el neón, el sodio, el magnesio, el aluminio, el silicio, el fósforo, el azufre, el cloro, el argón, el potasio, el calcio, el titanio, el hierro y el cobre.
Conclusión
El equilibrio eléctrico es un estado en el que los átomos tienen una carga equilibrada en su interior, lo que significa que tienen el mismo número de electrones que de protones. Este estado de equilibrio es importante para la estabilidad de los átomos y moléculas en la naturaleza y para el funcionamiento de los circuitos eléctricos y electrónicos.
Preguntas frecuentes
1. ¿Por qué es importante el equilibrio eléctrico?
El equilibrio eléctrico es importante para la estabilidad de los átomos y moléculas en la naturaleza y para el funcionamiento de los circuitos eléctricos y electrónicos.
2. ¿Cómo se logra el equilibrio eléctrico?
El equilibrio eléctrico se logra cuando un átomo tiene el mismo número de electrones que de protones.
3. ¿Cómo se mide el equilibrio eléctrico?
El equilibrio eléctrico se puede medir a través del potencial de ionización y la electronegatividad de los átomos.
4. ¿Qué átomos tienen carga equilibrada?
Algunos ejemplos de átomos con carga equilibrada son el hidrógeno, el helio, el litio, el berilio, el boro, el carbono, el nitrógeno, el oxígeno, el flúor, el neón, el sodio, el magnesio, el aluminio, el silicio, el fósforo, el azufre, el cloro, el argón, el potasio, el calcio, el titanio, el hierro y el cobre.
5. ¿Por qué los átomos con carga desequilibrada pueden causar reacciones químicas no deseadas o explosiones?
Si un átomo tiene una carga desequilibrada, puede atraer o repeler a otros átomos o moléculas cargados eléctricamente. Esto puede causar reacciones químicas no deseadas o incluso explosiones.
Deja una respuesta