Ley de conservación de la masa: ¡descubre su importancia!
La ley de conservación de la masa, también conocida como ley de Lavoisier, es una de las leyes fundamentales de la química. Esta ley establece que la masa de un sistema cerrado permanece constante, es decir, que la masa no se crea ni se destruye, solo se transforma.
Esta ley fue descubierta por el químico Antoine Lavoisier en el siglo XVIII, quien demostró que la cantidad total de masa en una reacción química es igual a la cantidad total de masa en los productos de la reacción. Por ejemplo, si se quema una hoja de papel, la masa de los productos de la combustión será igual a la masa de la hoja de papel antes de la combustión.
La importancia de la ley de conservación de la masa radica en que nos permite entender cómo se producen las reacciones químicas y cómo se pueden predecir los productos de una reacción. Además, esta ley se aplica en muchos campos de la ciencia, como la física, la biología y la geología.
A continuación, se describen algunos de los aspectos más importantes de la ley de conservación de la masa:
- Cómo se aplica la ley de conservación de la masa en la química
- Cómo se aplica la ley de conservación de la masa en la física
- Cómo se aplica la ley de conservación de la masa en la biología
- Cómo se aplica la ley de conservación de la masa en la geología
- Conclusión
-
Preguntas frecuentes
- ¿Por qué se llama ley de Lavoisier?
- ¿Cómo se puede demostrar la ley de conservación de la masa?
- ¿La ley de conservación de la masa se aplica solo en sistemas cerrados?
- ¿La ley de conservación de la masa se aplica en sistemas abiertos?
- ¿La ley de conservación de la masa se aplica en sistemas donde hay reacciones nucleares?
Cómo se aplica la ley de conservación de la masa en la química
La ley de conservación de la masa se aplica en la química para predecir los productos de una reacción química. Para ello, es necesario conocer la estequiometría de la reacción, es decir, la relación entre las cantidades de reactantes y productos en la reacción.
Por ejemplo, si se quiere saber cuántos gramos de dióxido de carbono se producirán al quemar 10 gramos de metano, se debe conocer la ecuación química de la reacción y la estequiometría de la misma. La ecuación química de esta reacción es:
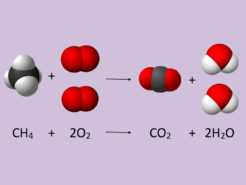
CH4 + 2O2 → CO2 + 2H2O
La estequiometría indica que por cada mol de metano que se quema, se producen un mol de dióxido de carbono y dos moles de agua. Por lo tanto, si se queman 10 gramos de metano, se producirán 22,4 gramos de dióxido de carbono.
Cómo se aplica la ley de conservación de la masa en la física
La ley de conservación de la masa también se aplica en la física, especialmente en el estudio de la mecánica y la termodinámica. Por ejemplo, en la mecánica, esta ley se aplica para calcular la cantidad de energía cinética y potencial en un sistema cerrado.
En la termodinámica, la ley de conservación de la masa se aplica para entender cómo se produce y se transfiere el calor en un sistema cerrado. Además, esta ley se utiliza para calcular la cantidad de trabajo que se realiza en un sistema cerrado.
Cómo se aplica la ley de conservación de la masa en la biología
En la biología, la ley de conservación de la masa se aplica para entender cómo se producen y se transforman los nutrientes en los sistemas biológicos. Por ejemplo, esta ley se aplica para entender cómo se transforma la glucosa en energía en las células.
Además, esta ley se utiliza para entender los procesos de crecimiento y desarrollo de los organismos, así como para calcular la cantidad de nutrientes que se deben consumir para mantener una dieta saludable.
Cómo se aplica la ley de conservación de la masa en la geología
En la geología, la ley de conservación de la masa se aplica para entender cómo se producen y se transforman los materiales en la Tierra. Por ejemplo, esta ley se aplica para entender cómo se forman las rocas y los minerales a partir de los procesos geológicos.
Además, esta ley se utiliza para entender cómo se producen los terremotos y las erupciones volcánicas, así como para calcular la cantidad de energía que se libera en estos eventos.
Conclusión
La ley de conservación de la masa es una de las leyes fundamentales de la química que nos permite entender cómo se producen y se transforman los materiales en los sistemas cerrados. Esta ley se aplica en muchos campos de la ciencia, como la física, la biología y la geología, y nos ayuda a predecir los productos de una reacción química, entender los procesos biológicos y geológicos, y calcular la cantidad de energía y trabajo que se realiza en un sistema cerrado.
Preguntas frecuentes
¿Por qué se llama ley de Lavoisier?
La ley de conservación de la masa se llama así en honor al químico francés Antoine Lavoisier, quien la descubrió en el siglo XVIII.
¿Cómo se puede demostrar la ley de conservación de la masa?
La ley de conservación de la masa se puede demostrar mediante experimentos en los que se mide la masa de los productos antes y después de una reacción química.
¿La ley de conservación de la masa se aplica solo en sistemas cerrados?
Sí, la ley de conservación de la masa se aplica solo en sistemas cerrados, es decir, en sistemas en los que no hay intercambio de masa con el exterior.
¿La ley de conservación de la masa se aplica en sistemas abiertos?
No, la ley de conservación de la masa no se aplica en sistemas abiertos, ya que en estos sistemas puede haber intercambio de masa con el exterior.
¿La ley de conservación de la masa se aplica en sistemas donde hay reacciones nucleares?
Sí, la ley de conservación de la masa se aplica también en sistemas donde hay reacciones nucleares, ya que se conserva la cantidad total de masa en el sistema cerrado.
Deja una respuesta