Secretos de la química: ¿qué determina la formación de compuestos?
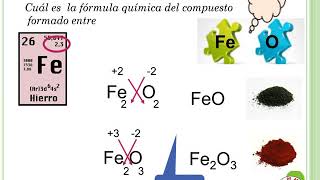
La química es una ciencia fascinante que estudia la composición, estructura y propiedades de la materia. Uno de los aspectos más interesantes de la química es la formación de compuestos, que son sustancias formadas por la combinación de dos o más elementos químicos. Pero ¿qué determina la formación de compuestos? En este artículo, vamos a explorar los secretos de la química detrás de la formación de compuestos.
Los elementos químicos y su estructura
Antes de adentrarnos en la formación de compuestos, es importante entender la estructura de los elementos químicos. Cada elemento químico está formado por átomos, que a su vez están compuestos por protones, neutrones y electrones. Los protones y neutrones se encuentran en el núcleo del átomo, mientras que los electrones orbitan alrededor del núcleo.
La estructura de los átomos determina las propiedades de los elementos químicos. Por ejemplo, el número de protones en el núcleo de un átomo determina su número atómico, que a su vez determina su posición en la tabla periódica de los elementos. Los elementos químicos con propiedades similares se encuentran en la misma columna de la tabla periódica.
La formación de compuestos
Los compuestos se forman cuando dos o más elementos químicos se combinan químicamente. Para que la combinación sea posible, los elementos deben tener propiedades químicas compatibles. Por ejemplo, los elementos deben tener una afinidad química similar, lo que significa que deben tener una tendencia a reaccionar juntos.
La formación de compuestos implica la transferencia o el intercambio de electrones entre los átomos de los elementos que se combinan. Los electrones de un átomo pueden ser atraídos por los protones del núcleo de otro átomo, lo que resulta en la formación de un enlace químico entre los dos átomos. Los enlaces químicos pueden ser covalentes, iónicos o metálicos, dependiendo de la naturaleza de los átomos involucrados.
La importancia de los enlaces químicos
Los enlaces químicos son fundamentales para la formación de compuestos y para las propiedades de los compuestos resultantes. Los enlaces covalentes implican el intercambio de electrones entre los átomos, lo que resulta en la formación de moléculas estables. Los compuestos covalentes son típicamente sólidos, líquidos o gases a temperatura ambiente, y tienen puntos de fusión y ebullición relativamente bajos.
Los enlaces iónicos implican la transferencia de electrones de un átomo a otro, lo que resulta en la formación de iones cargados positiva y negativamente. Los compuestos iónicos tienen un alto punto de fusión y ebullición, y son típicamente sólidos cristalinos a temperatura ambiente.
Los enlaces metálicos implican la compartición de electrones de valencia entre muchos átomos, lo que resulta en la formación de una estructura cristalina. Los compuestos metálicos son conductores de electricidad y tienen puntos de fusión y ebullición relativamente altos.
Las leyes de la química
La formación de compuestos está gobernada por varias leyes de la química, que describen la relación entre los elementos y sus compuestos. La ley de la conservación de la masa establece que la masa total de los reactantes en una reacción química es igual a la masa total de los productos. La ley de las proporciones definidas establece que los compuestos químicos siempre contienen los mismos elementos en las mismas proporciones.
La ley de las proporciones múltiples establece que cuando dos elementos forman más de un compuesto, la proporción de masa de uno de los elementos que se combina con una masa fija del otro elemento está en una relación de números enteros pequeños.
Conclusiones
La formación de compuestos es un proceso fascinante que está gobernado por las propiedades químicas de los elementos que se combinan. Los enlaces químicos son fundamentales para la formación de compuestos y para las propiedades de los compuestos resultantes. Las leyes de la química describen la relación entre los elementos y sus compuestos, y son esenciales para comprender la química.
Preguntas frecuentes
1. ¿Por qué los elementos químicos se combinan para formar compuestos?
Los elementos químicos se combinan para formar compuestos porque tienen propiedades químicas compatibles. Los elementos deben tener una afinidad química similar, lo que significa que deben tener una tendencia a reaccionar juntos.
2. ¿Qué son los enlaces químicos?
Los enlaces químicos son las fuerzas que mantienen unidos a los átomos en los compuestos químicos. Los enlaces pueden ser covalentes, iónicos o metálicos, dependiendo de la naturaleza de los átomos involucrados.
3. ¿Qué son las leyes de la química?
Las leyes de la química describen la relación entre los elementos y sus compuestos. Las leyes incluyen la ley de la conservación de la masa, la ley de las proporciones definidas y la ley de las proporciones múltiples.
4. ¿Qué son los compuestos iónicos?
Los compuestos iónicos son compuestos químicos que se forman por la transferencia de electrones de un átomo a otro. Los compuestos iónicos tienen un alto punto de fusión y ebullición, y son típicamente sólidos cristalinos a temperatura ambiente.
5. ¿Por qué son importantes los enlaces químicos?
Los enlaces químicos son fundamentales para la formación de compuestos y para las propiedades de los compuestos resultantes. Los enlaces covalentes implican el intercambio de electrones entre los átomos, lo que resulta en la formación de moléculas estables. Los enlaces iónicos implican la transferencia de electrones de un átomo a otro, lo que resulta en la formación de iones cargados positiva y negativamente. Los enlaces metálicos implican la compartición de electrones de valencia entre muchos átomos, lo que resulta en la formación de una estructura cristalina.
Deja una respuesta